题目内容
如图所示是常见单质及其化合物的转化关系(有关反应的条件及生成的H2O已略去).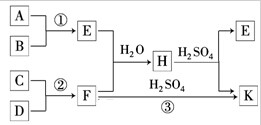
已知:
a.A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
b.反应①、②是化工生产中的重要反应.
c.化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
请按要求填空:
(1)反应③的化学方程式为 ;
(2)F的化学式: ,H的化学式: ;
(3)H的溶液与稀硫酸反应的离子方程式: .

已知:
a.A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
b.反应①、②是化工生产中的重要反应.
c.化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
请按要求填空:
(1)反应③的化学方程式为
(2)F的化学式:
(3)H的溶液与稀硫酸反应的离子方程式:
考点:无机物的推断
专题:推断题
分析:由短周期元素的单质及其化合物的转化关系图可知,化合物E是形成酸雨的污染物之一,则E为SO2,A、B、C、D都是非金属单质,其中B、C、D在常温常压下是气体,则A为S,B为O2;化合物K是常用的氮肥,K为硫酸铵,所以F为氨气,则C、D分别为N2、H2,以此解答该题.
解答:
解:由短周期元素的单质及其化合物的转化关系图可知,化合物E是形成酸雨的污染物之一,则E为SO2,A、B、C、D都是非金属单质,其中B、C、D在常温常压下是气体,则A为S,B为O2;化合物K是常用的氮肥,K为硫酸铵,所以F为氨气,则C、D分别为N2、H2,
(1)该反应为氨气与硫酸反应生成硫酸铵,化学反应为2NH3+H2SO4═(NH4)2SO4,
故答案为:2NH3+H2SO4═(NH4)2SO4;
(2)F为NH3,H为二氧化硫与氨气在水中的反应,反应生成(NH4)2SO3或NH4HSO3,故答案为:NH3;(NH4)2SO3或NH4HSO3;
(3)H为(NH4)2SO3或NH4HSO3,与硫酸反应的离子方程式为SO32-+2H+=SO2↑+H2O或HSO3-+H+=SO2↑+H2O,
故答案为:SO32-+2H+=SO2↑+H2O或HSO3-+H+=SO2↑+H2O.
(1)该反应为氨气与硫酸反应生成硫酸铵,化学反应为2NH3+H2SO4═(NH4)2SO4,
故答案为:2NH3+H2SO4═(NH4)2SO4;
(2)F为NH3,H为二氧化硫与氨气在水中的反应,反应生成(NH4)2SO3或NH4HSO3,故答案为:NH3;(NH4)2SO3或NH4HSO3;
(3)H为(NH4)2SO3或NH4HSO3,与硫酸反应的离子方程式为SO32-+2H+=SO2↑+H2O或HSO3-+H+=SO2↑+H2O,
故答案为:SO32-+2H+=SO2↑+H2O或HSO3-+H+=SO2↑+H2O.
点评:本题考查无机物的推断,利用物质的性质及转化关系图来推断出各物质是解答本题的关键,(3)中的离子反应为解答的易错点,注意结合氧化还原反应来解答,题目难度中等.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g)?xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
| A、平衡时,甲、乙两容器中A、B的物质的量之比不相等 |
| B、若平衡时,甲、乙两容器中A的物质的量相等,则x=2 |
| C、平衡时甲中A的体积分数为40% |
| D、若平衡时两容器中的压强不相等,则两容器中压强之比为5:8 |
向饱和澄清石灰水中加入少量CaC2(实验室常用CaC2制乙炔),充分反应后恢复到原来的温度,所得溶液中( )
| A、Ksp[Ca(OH)2]增大 |
| B、c(Ca2+)、c(OH-)均保持不变 |
| C、氢氧化钙的溶解度增大 |
| D、c(OH-)增大、c(H+)减小 |
常温下,在含有H+,SO42-,Fe2+的溶液中,加入含下列离子的溶液后,溶液中的各种离子仍能大量共存的是( )
| A、MnO4- |
| B、CH3COO- |
| C、S2O32- |
| D、Br- |
在某容积为2L的密闭容器内,加入0.2mol的CO和0.2mol 的H2O,在催化剂存在的条件下某高温加热,发生如下反应:
CO(g)+H2O(g)?CO2(g)+H2(g)△H=a kJ?mol(a>0)反应达到平衡后,测得 c(CO):c(CO2)=3:2.下列说法不正确的是( )
CO(g)+H2O(g)?CO2(g)+H2(g)△H=a kJ?mol(a>0)反应达到平衡后,测得 c(CO):c(CO2)=3:2.下列说法不正确的是( )
| A、平衡时CO的转化率为40% | ||
| B、反应放出的热量为0.08 akJ | ||
C、该温度下的化学平衡常数为
| ||
| D、若将容器的体积压缩为1 L,CO的平衡浓度变为0.12 mol/L |