题目内容
17.已知乙烯能发生以下转化关系:
试回答下列问题:
(1)乙烯的电子式为
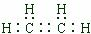 ;B中含官能团名称是羟基.
;B中含官能团名称是羟基.(2)写出反应的化学方程式
①CH2=CH2+H2O$\stackrel{一定条件}{→}$$\frac{\underline{\;一定条件\;}}{\;}$CH3CH2OH,反应类型:加成反应;
②2CH3CH2OH+O2$→_{△}^{Cu/Ag}$2CH3CHO+2H2O,反应类型:氧化反应;
④CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,反应类型:酯化或取代反应.
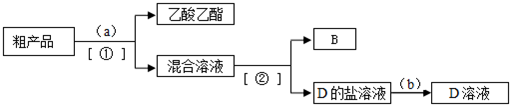
(3)现拟分离含B、D和水的乙酸乙酯粗产品,下图是分离操作流程,请在图中圆括号内
填入适当的试剂,在方括号内填入适当的分离方法.
试剂a是饱和碳酸钠溶,b是浓硫酸(或硫酸或盐酸等);分离方法①是分液,②是蒸馏;
(4)与B和D在浓硫酸催化作用下发生反应相似,B的同系物X也能和D发生反应生成酯Y,Y的分子量比乙酸乙酯大28,则X的分子式为C4H10O.
分析 乙烯与水发生加成反应生成B为CH3CH2OH,乙醇在Cu作催化剂条件下发生氧化反应生成C为CH3CHO,B与D反应生成乙酸乙酯(CH3COOCH2CH3),则D为CH3COOH,
乙酸乙酯不溶于饱和碳酸钠溶液,乙醇乙溶于水,乙酸可与碳酸钠反应,可用分液的方法分离,混合溶液蒸馏得到B为乙醇,D的盐溶液加入酸得到乙酸溶液,以此解答该题.
解答 解:乙烯与水发生加成反应生成B为CH3CH2OH,乙醇在Cu作催化剂条件下发生氧化反应生成C为CH3CHO,B与D反应生成乙酸乙酯(CH3COOCH2CH3),则D为CH3COOH,
(1)乙烯的电子式为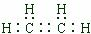 ,B为乙醇,含有的官能团为羟基,故答案为:
,B为乙醇,含有的官能团为羟基,故答案为: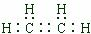 ; 羟基;
; 羟基;
(2)①乙烯和水发生加成反应生成乙醇,方程式为CH2=CH2+H2O $\stackrel{一定条件}{→}$ $\frac{\underline{\;一定条件\;}}{\;}$CH3CH2OH,
故答案为:CH2=CH2+H2O $\stackrel{一定条件}{→}$ $\frac{\underline{\;一定条件\;}}{\;}$CH3CH2OH;加成反应;
②乙醇在铜催化作用下与氧气发生反应生成乙醛,发生氧化反应,方程式为2CH3CH2OH+O2$→_{△}^{Cu/Ag}$ 2 CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu/Ag}$ 2 CH3CHO+2H2O;氧化反应;
④乙醇、乙酸在浓硫酸作用下发生酯化反应生成乙酸乙酯,方程式为CH3CH2OH+CH3COOH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,应为取代反应,
故答案为:CH3CH2OH+CH3COOH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O; 酯化或取代反应;
(3)乙酸乙酯不溶于饱和碳酸钠溶液,乙醇乙溶于水,乙酸可与碳酸钠反应,可用分液的方法分离,混合溶液蒸馏得到B为乙醇,D的盐溶液加入浓硫酸(或硫酸或盐酸等)得到乙酸溶液,
故答案为:饱和碳酸钠溶液;浓硫酸(或硫酸或盐酸等);分液; 蒸馏;
(4)与B和D在浓硫酸催化作用下发生反应相似,B的同系物X也能和D发生反应生成酯Y,Y的分子量比乙酸乙酯大28,X应为丁醇,相差2个CH2,分子式为C4H10O,
故答案为:C4H10O.
点评 本题考查有机物推断,为高频考点,侧重学生的分析能力的考查,注意把握烯与醇、醛、羧酸之间的转化,难度不大,注意基础知识的理解掌握.

| A. | 过氧化钠、二氧化硫属于氧化物,而次氯酸属于弱酸,臭氧属于单质 | |
| B. | 它们都能使品红溶液褪色,但褪色原理不同;加热褪色的溶液都能变红 | |
| C. | 二氧化硫能与其他三种物质发生氧化还原反应,二氧化硫表现还原性 | |
| D. | 过氧化钠溶于水产生的气体与臭氧互为同素异形体,臭氧比氧气活泼 |
| A. | 手机上用的锂离子电池属于二次电池 | |
| B. | 铜锌原电池工作时,电子从铜电极流向锌电极 | |
| C. | 氢氧燃料电池可把化学能转化为电能 | |
| D. | 锌锰干电池中,锌电极是负极 |
| A. | C | B. | Si | C. | S | D. | Cl |
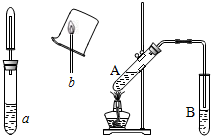 乙醇性质探究
乙醇性质探究 }及阻燃剂四溴双酚A.合成线路如下:
}及阻燃剂四溴双酚A.合成线路如下: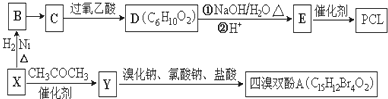
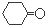

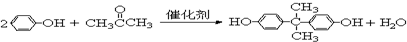 .
.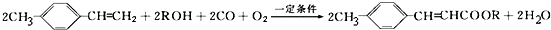
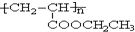 ,写出合成该涂料的反应流程图:
,写出合成该涂料的反应流程图: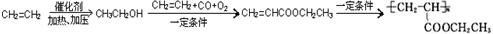 .
.