题目内容
6.设NA为阿伏加德罗常数的值,下列各项叙述正确的是( )①1molCl2参加反应转移电子数一定为2NA
②1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA
③标准状况下,44.8L NO与22.4LO2混合后气体中分子总数为2NA
④1L 2mol•L-1的Al(NO3)3溶液中含Al3+个数为2NA
⑤1L 2mol/L的氯化铁溶液完全制成胶体,氢氧化铁胶体的粒子数小于2NA
⑥6.0g SiO2晶体中含有的硅氧键数目为0.4NA
⑦1molCH5+所含的电子数为10NA
⑧在标准状况下,2.8g N2和2.8g CO所含电子数均为1.4NA
⑨300mL 2mol/L蔗糖溶液中所含分子数为0.6NA
⑩标准状况下,2.24L乙醇分子所含的C-H键数为 0.5NA.
| A. | ②③⑦⑧⑨⑩ | B. | ①②③⑤⑧⑨ | C. | ②⑤⑥⑦⑧ | D. | ②④⑦⑧⑩ |
分析 ①根据Cl2参加反应后的价态来分析;
②Na2O和Na2O2均由2个阳离子和1个阴离子构成;
③NO2气体中存在平衡:2NO2?N2O4;
④Al3+是弱碱阳离子,在溶液中会水解;
⑤一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
⑥求出6.0g SiO2晶体的物质的量,然后根据1mol二氧化硅中4molSi-O键来分析;
⑦CH5+为10电子微粒;
⑧2.8g N2和2.8g CO的物质的量均为0.1mol,且两者中均含14个电子;
⑨蔗糖溶液中除了蔗糖分子,还含水分子;
⑩标准状况下,乙醇为液态.
解答 解:①由于Cl2参加反应后的价态不能确定,故1mol氯气反应后转移的电子数无法确定,故错误;
②Na2O和Na2O2均由2个阳离子和1个阴离子构成,故1mol混合物中含3mol离子即3NA个,故正确;
③标准状况下,44.8L NO与22.4LO2混合后生成2molNO2,但NO2气体中存在平衡:2NO2?N2O4,故混合后气体中分子总数小于2NA,故错误;
④Al3+是弱碱阳离子,在溶液中会水解,故溶液中的铝离子的个数小于2NA个,故错误;
⑤一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故所得的氢氧化铁胶粒的个数小于2NA个,故正确;
⑥求出6.0g SiO2晶体的物质的量,而1mol二氧化硅中4molSi-O键,故0.1mol二氧化硅中含0.4mol硅氧键即0.4NA个,故正确;
⑦CH5+为10电子微粒,故1mol中含10mol电子即10NA个,故正确;
⑧2.8g N2和2.8g CO的物质的量均为0.1mol,且两者中均含14个电子,故0.1mol两者中均含1.4mol电子即1.4NA个,故正确;
⑨蔗糖溶液中除了蔗糖分子,还含水分子,故溶液中的分子个数大于0.6NA个,故错误;
⑩标准状况下,乙醇为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

 快乐5加2金卷系列答案
快乐5加2金卷系列答案| A. | 随着温度的升高,碳酸溶液的pH减小 | |
| B. | 随着温度的升高,纯水的pH减小 | |
| C. | 新氯水制经光照一段时间后,pH减小 | |
| D. | 氢氧化钠溶液久置于空气中,pH增大 |
| A. | 甲烷、CO合成乙酸乙酯:2CH4+2CO$\stackrel{催化剂}{→}$CH3COOCH2CH3 | |
| B. | 烯烃与水煤气发生的羰基合成反应:RCH═CH2+CO+H2$\stackrel{催化剂}{→}$RCH2CH2CHO | |
| C. | 葡萄糖在酒化酶作用下转化为酒精 | |
| D. | 氯乙烯合成聚氯乙烯 |
| A. | 镁和锌分别与相同浓度的盐酸反应,镁产生H2的速率快 | |
| B. | 铜与浓硝酸反应生成NO2,与稀硝酸反应生成NO | |
| C. | 用加热的方法可以将水中溶解的O-和N2赶出 | |
| D. | 面粉加工厂内充满粉尘,遇火易发生爆炸 |
| A. | O2-的结构示意图: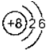 | |
| B. | 四氯化碳的电子式: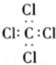 | |
| C. | HClO的结构式为:H-O-Cl | |
| D. | 用电子式表示氯化氢分子的形成过程: |
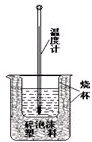 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题:
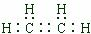 ;B中含官能团名称是羟基.
;B中含官能团名称是羟基.