题目内容
6.下列化合物不属于有机物的是( )| A. | CH3CH2OH | B. | CH3COOH | C. | CH3COOCH3 | D. | CO2 |
分析 根据含有碳元素的化合物叫有机化合物,简称有机物;碳的氧化物、碳酸盐、碳酸、氰化物,氰酸盐虽含碳虽含碳,但其性质与无机物类似,因此把它们看作无机物;据此进行分析判断.
解答 解:A.乙醇是由C、H、O三种元素组成的有机物,故A错误;B.乙酸是由C、H、O三种元素组成的羧酸,属于有机物,故B错误;C.元素甲酯属于有机物,故C错误;D.二氧化碳中虽然含有碳元素,但是其性质与无机物类似,属于无机物,故D正确,故选D.
点评 本题考查有机物的概念,难度不大,掌握有机物与无机物的概念、特征等是正确解答此类题的关键.

练习册系列答案
相关题目
16.NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 0.1molC3H6Cl2中化学键总数为NA | |
| B. | 14g乙烯和丙烯混合气体中含原子数为3NA | |
| C. | 标准状况下,1L苯完全燃烧生成的气态产物的分子数为$\frac{6}{22.4}$NA | |
| D. | 0.1NA乙醇分子完全燃烧所消耗的氧气为0.3mol |
17.下列二者之间是同分异构体关系的是( )
| A. | 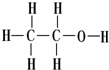 和 和 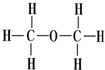 | B. | 金刚石和石墨 | C. | 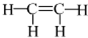 和H-C≡C-H 和H-C≡C-H | D. | O3和O2 |
14.下列物质的类别与所含官能团都正确的是( )
| A. | 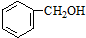 酚类-OH 酚类-OH | B. | 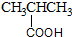 羧酸-COOH 羧酸-COOH | C. |  醛类-CHO 醛类-CHO | D. | CH3OCH3 醚类 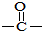 |
1.下列关于F、Cl、Br、I性质的比较,不正确的是( )
| A. | 单质的颜色随核电荷数的增加而加深 | |
| B. | 单质的熔、沸点随核电荷数的增加而升高 | |
| C. | 单质的氧化性减弱 | |
| D. | 它们的氢化物的稳定性随核电荷数的增加而增强 |
11.下表为元素周期表的一部分用元素符号、离子符号或化学式回答下列问题.
(1)在上表所列出的短周期元素中,原子半径最小的是F(除稀有气体元素);形成的气态氢化物最稳定的是HF;最高价氧化物对应的水化物中酸性最强的是HClO4;简单阳离子半径最小的是Al3+.
(2)写出④与⑧元素组成的分子的电子式: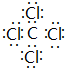 ,该分子含有极性(填“极性”或“非极性”)键;⑤元素形成的单质的结构式为N≡N⑧元素形成简单离子的结构示意图为
,该分子含有极性(填“极性”或“非极性”)键;⑤元素形成的单质的结构式为N≡N⑧元素形成简单离子的结构示意图为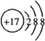 .
.
(3)②与⑧形成的化合物溶于水所克服的微粒间作用力为离子键.
(4)①②③几种元素最高价氧化物对应的水化物碱性最强的是KOH,元素①单质和⑥的氢化物反应的化学方程式为2K+2H2O=2KOH+H2↑.
(5)⑦⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 3 | ② | ③ | ⑧ | ⑩ | ||||
| 4 | ① | ⑨ |
(2)写出④与⑧元素组成的分子的电子式:
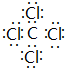 ,该分子含有极性(填“极性”或“非极性”)键;⑤元素形成的单质的结构式为N≡N⑧元素形成简单离子的结构示意图为
,该分子含有极性(填“极性”或“非极性”)键;⑤元素形成的单质的结构式为N≡N⑧元素形成简单离子的结构示意图为 .
.(3)②与⑧形成的化合物溶于水所克服的微粒间作用力为离子键.
(4)①②③几种元素最高价氧化物对应的水化物碱性最强的是KOH,元素①单质和⑥的氢化物反应的化学方程式为2K+2H2O=2KOH+H2↑.
(5)⑦⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-.
18.粗盐中含有不溶性泥沙,可溶性的CaCl2、MgCl2以及一些硫酸盐等.精制食盐水的实验操作顺序如下:①加入过量BaCl2溶液,②加入过量NaOH溶液,③加入过量Na2CO3溶液,④过滤,⑤加入适量盐酸.下列说法不正确的是( )
| A. | ①②③中加入过量的试剂是为了完全除去相应的杂质离子 | |
| B. | ③中加入过量Na2CO3溶液仅为了完全除去Ca2+ | |
| C. | 因为Mg(OH)2难溶而MgCO3微溶,所以用NaOH除Mg2+效果比用Na2CO3好 | |
| D. | ⑤中可以通过边滴加边测定溶液pH的方法,控制加入的盐酸“适量” |
15.下列关于卤素的叙述说法错误的是( )
| A. | 单质的颜色随核电荷数的增加逐渐加深 | |
| B. | 元素的最高化合价均为+7 | |
| C. | 从上到下原子半径递增 | |
| D. | 从上到下非金属性减弱 |
16.常温下,某无色透明的溶液中,下列各组离子能够大量共存的是( )
| A. | H+、Na+、Cl-、HCO3- | B. | Ba2+、Na+、SO42-、Cl- | ||
| C. | MnO4-、K+、S2-、H+ | D. | Mg2+、Cl-、NO${\;}_{3}^{-}$、H+ |