题目内容
3.下列有关离子检验的操作和实验结论正确的是( )| A. | 向某溶液加入NaOH并微热,产生能够使湿润的红色石蕊试纸变蓝的无色气体,该溶液中一定含有NH4+ | |
| B. | 向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有SO42- | |
| C. | 向某溶液中加入氨水,产生白色沉淀,则该溶液中一定含有Mg2+ | |
| D. | 用铂丝蘸取某溶液在酒精灯火焰上灼烧,若火焰呈黄色,则证明该溶液中无K+离子 |
分析 A.铵盐与碱反应生成氨气,能使湿润的红色石蕊试纸变蓝;
B.AgCl也为不溶于酸的白色沉淀;
C.原溶液中可能含有铝离子,不一定含有镁离子;
D.观察钾离子的焰色反应的颜色需要透过蓝色钴玻璃.
解答 解:A.铵盐与碱反应生成氨气,能使湿润的红色石蕊试纸变蓝,则向某溶液加入NaOH并微热,产生能够使湿润的红色石蕊试纸变蓝的无色气体,该溶液中一定含有NH4+,故A正确;
B.某溶液中加入氯化钡溶液,有白色沉淀生成,再加盐酸酸化,沉淀不溶解,该溶液中可能含有SO42-或Ag+,但二者不能同时存在,故B错误;
B.向某溶液中加入氨水,产生白色沉淀,该沉淀可能为氢氧化铝,则该溶液中可能含有铝离子,不一定含有Mg2+,故C错误;
C.向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体,气体可能为二氧化硫或二氧化碳,则溶液中可能存在HCO3-、SO32-、HSO3-、CO32-,故C错误;
D.用铂丝蘸取某溶液在酒精灯火焰上灼烧,若火焰呈黄色,溶液中一定含有钠离子,观察钾离子的焰色反应时需要透过蓝色钴玻璃,则无法判断该溶液中是否含有K+离子,故D错误;
故选A.
点评 本题考查常见离子的检验方法,题目难度中等,熟悉常见离子的检验方法是解答本题的关键,注意检验离子时应排除其它离子的干扰,确保检验方案的严密性,试题培养了学生的化学实验能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列说法一定正确的是( )
| A. | 反应A(s)?2B(g)+C(g),当C的体积分数不变时,反应达到平衡状态 | |
| B. | 将钢闸门与直流电源的正极相连,可防止钢闸门腐蚀 | |
| C. | 用FeS为沉淀剂除去废水中的Hg2+:FeS(s)+Hg2+(aq)═HgS(s)+Fe2+(aq) | |
| D. | 增大反应物浓度可加快反应速率,因此可用浓硫酸与铁反应增大生成氢气的速率 |
14.下列装置工作时,将化学能转化为电能的是( )
| A. |  燃气灶 | B. |  硅太阳能电池 | C. |  铅蓄电池 | D. |  风力发电机 |
8.下列化学用语的书写正确的是( )
| A. | 基态Mg原子的核外电子排布图: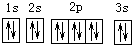 | |
| B. | 过氧化氢的电子式: | |
| C. | As原子的简化电子排布式:[Ar]4s24p3 | |
| D. | 羟基的电子式: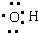 |
15.标准状况下,将15.68LCO2与500mL2mol/L的NaOH溶液充分反应,生成了Na2CO3和NaHCO3,再将溶液蒸干充分灼烧,得到的固体物质质量为( )
| A. | 84g | B. | 65.4g | C. | 67.6g | D. | 53g |
12.关于硅及其化合物的叙述错误的是( )
| A. | 单质硅是良好的半导体材料 | |
| B. | 硅酸比碳酸酸性弱,故二氧化硅不能与碳酸钠反应 | |
| C. | 氢氟酸可以用来雕刻玻璃 | |
| D. | 玻璃、水泥、陶瓷都属于硅酸盐产品 |
13.关于反应:①2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
③CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
下列叙述正确的是( )
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
③CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
下列叙述正确的是( )
| A. | CO的燃烧热为-566 kJ/mol | |
| B. | 在③反应时,若加入催化剂,可以使△H减小 | |
| C. | 若投入1molCO2和3molH2在一定条件下充分反应,则放出热量49 kJ | |
| D. | 若生成相同质量的CO2,则放出的热量C2H2大于CO |