题目内容
6.镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.反应中镁和铝的关系说法正确的是( )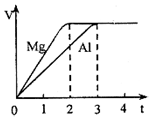
| A. | 物质的量之比为3:2 | B. | 质量之比为3:4 | ||
| C. | 摩尔质量之比为9:8 | D. | 体积之比为2:3 |
分析 根据图象可知,两种金属得到的氢气一样多,然后根据金属镁、铝和足量的稀硫酸反应的化学方程式:Mg+H2SO4=MgSO4+H2↑,2Al+3H2SO4=Al2(SO4)3+3H2↑,即可找出各个量之间的关系.
解答 解:A、由于Mg~H2,2Al~3H2,且两种金属得到的氢气一样多,因此镁和铝的物质的量的比是1:$\frac{2}{3}$=3:2,故A正确;
B、由于Mg~H2,2Al~3H2,且两种金属得到的氢气一样多,因此镁和铝的物质的量的比是1:$\frac{2}{3}$=3:2,则它们的质量的比为(3×24):(2×27)=4:3,故B错误;
C、镁和铝的摩尔质量之比和该化学反应毫无关系,即它们的摩尔质量之比为24g/mol:27g/mol=8:9,故C错误;
D、根据B的分析,金属镁和铝的质量的比为(3×24):(2×27)=4:3,体积等于质量和密度之比,所以金属的体积之比还得借助密度数据计算,故D错误;
故选A.
点评 本题以图象形式考查混合物计算、金属与酸的反应,侧重考查学生分析计算能力,明确反应方程式中各个物理量之间的关系是解本题关键,题目难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
16.在1×105Pa和298K时,将1mol气态AB分子分离成气态A原子和B原子所需要的能量称为键能(kJ•mol-1).下面是一些共价键的键能:(已知氨分子中有三个等价的氮氢共价键)
①在1×105Pa、298K时,取一定量的 N2和H2放入一密闭容器中,在催化剂存在下进行反应:N2+H2?NH3,生成2molNH3,该过程中,断键吸收(填“释放”或“吸收”)能量2254KJ,成键释放(填“释放”或“吸收”)能量2346KJ;据此判断工业合成氨的反应是放热反应(填“吸热”或“放热”);
②若将1mol N2和3mol H2放入一密闭容器中在催化剂存在下进行反应,理论上放出或吸收的热量为Q1,而在实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是A.
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2.
| 共价键 | H-H | N≡N | N-H |
| 键能(kJ•mol-1) | 436 | 945 | 391 |
②若将1mol N2和3mol H2放入一密闭容器中在催化剂存在下进行反应,理论上放出或吸收的热量为Q1,而在实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是A.
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2.
17.下列金属氧化物中,一般不用铝热反应来进行难熔金属冶炼的是( )
| A. | MnO2 | B. | Fe3O4 | C. | MgO | D. | Cr2O3 |
14.常温下,在0.10mol•L-1NaX溶液中水的电离度为a1,在0.10mol•L-1HCl溶液中,水的电离度为a2.若a1/a2=108,则0.10mol•L-1NaX溶液的pH是( )
| A. | 5 | B. | 7 | C. | 8 | D. | 9 |
1.H++OH-=H2O表示下列哪组离子反应( )
| A. | Cu(OH)2与H2SO4 | B. | Ba(OH)2与H2SO4 | C. | Ba(OH)2与HCl | D. | KHSO4与Ba(OH)2 |
11.维生素是参与生物生长发育和新陈代谢所必须的物质,中学生每天需要补充一定量的维生素C.下列食品中维生素C含量最丰富的是( )
| A. | 植物油 | B. | 馒头 | C. | 牛肉 | D. | 橙子 |
18.在100mLHNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.6mol/L,向该溶液中加入足量的铜粉,加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为(反应前后溶液体积变化忽略不计)( )
| A. | 0.025 mol/L | B. | 0.30mol/L | C. | 0.36mol/L | D. | 0.45mol/L |
15.下列状态的物质,既能导电又属于电解质的是( )
| A. | 盐酸 | B. | NH3 | C. | 熔融的Al2O3 | D. | BaSO4晶体 |
 向大气中排放过量的二氧化碳是造成全球气候变暖的重要因素,所以二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向.
向大气中排放过量的二氧化碳是造成全球气候变暖的重要因素,所以二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向. ;将足量的C02通入下列溶液中,最终溶液变浑浊的是ce.
;将足量的C02通入下列溶液中,最终溶液变浑浊的是ce.