题目内容
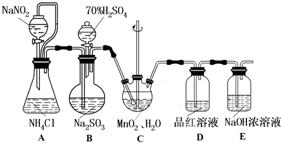
11.某兴趣小组模拟工业处理氨氮废水的原理,进行如下研究| 装置 | 操作 | 现象 |
 | 添加试剂,检查装置气密性,点燃酒精灯 | i.C中气体颜色变浅 ii.稍后,C中出现白烟并逐渐增多 |
(2)B中干燥管中应选用的药品为c(填字母)
a.无水 CuSO4 b.硅胶 c.碱石灰
(3)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)═N2(g)+6HCl(g)△H=-456kJ•mol-1
已知:

①NH3的电子式是
 .
.②断开1mol H-N键与断开1mol H-Cl键所需能量相差约为40KJkJ.
(4)现象ⅱ中产生白烟的化学方程式是HCl+NH3=NH4Cl
(5)某学生设计了如图装置以完成Cl2和NH3的反应.若该装置能实现设计目标,则

①石墨b电极上发生的是还原反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式:2NH3+6OH--6e-=N2+6H2O.
分析 (1)氯化铵和氢氧化钙加热发生复分解反应,生成氯化钙、氨气和水;
(2)用碱石灰干燥氨气;
(3)①氨气是氮原子和三个氢原子形成三个共价键,氮原子有一对孤对电子,据此书写电子式;
②化学反应的焓变=反应物键能总和-生成物键能总和计算;依据原子半径分析,键越短键越牢固;
(4)氨气被氯气氧化生成氮气和氯化氢,氨气过量和生成的氯化氢反应生成固体氯化铵白色固体颗粒;
(5)装置为原电池反应,钠离子移向可知a为负极,氨气失电子生成氮气,b为正极,氯气得到电子生成氯离子.
解答 解:(1)A中是氯化铵和氢氧化钙加热发生复分解反应,生成氯化钙、氨气和水,方程式为:化学反应方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
故答案为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
(2)氨气用碱石灰干燥,所以B中干燥管中应选用的药品为碱石灰;
故选c;
(3)①氨气中氮原子和3个氢原子形成3个共价键,氮原子有1对孤对电子,电子式为: ;
;
故答案为: ;
;
②焓变=反应物键能总和-生成物键能总和,6×(H-N)+3Cl-Cl-[6(H-Cl)+N≡N]=-456kJ•mol-1;得到6×(H-N)+3×243KJ/mol-[6(H-Cl)+945KJ/mol]=-456kJ•mol-1;得到6×(H-N)-6(H-Cl)=-456kJ•mol-1-3×243KJ/mol+945KJ/mol;(H-N)-(H-Cl)=-40KJ/mol,断开1mol H-N键与断开1mol H-Cl键所需能量相差约为40KJ;
故答案为:40KJ;
(4)氨气被氯气氧化生成氮气和氯化氢,3Cl2+2NH3=N2+6HCl,氨气过量和生成的氯化氢反应生成固体氯化铵白色固体颗粒,方程式为NH3+HCl=NH4Cl;
故答案为:HCl+NH3=NH4Cl;
(5)①装置为原电池反应,钠离子移向可知a为负极,氨气失电子生成氮气,b为正极,氯气得到电子生成氯离子,发生还原反应;
故答案为:还原;
②石墨a电极为负极,氨气失电子生成氮气,碱溶液中电极反应式为2NH3+6OH--6e-=N2+6H2O;
故答案为:2NH3+6OH--6e-=N2+6H2O.
点评 本题考查了物质性质与应用,键能和焓变的计算依据和方法,原电池电极反应书写方法,掌握物质性质和反应原理是解题关键,题目难度中等.

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案| A. | 气体的密度不再变化 | B. | NH3和 NO 的反应速率相等 | ||
| C. | 反应速率不再变化 | D. | NO 和H2O 浓度比不再变化 |
 (1)已知:①C(s)+O2(g)=CO2(g)△H=a kJ•mol-1
(1)已知:①C(s)+O2(g)=CO2(g)△H=a kJ•mol-1②2CO(g)+O2(g)=2CO2(g)△H=b kJ•mol-1;
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g)△H=c kJ•mol-1;
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H=c+2a-bkJ•mol-1.(用含a、b、c的式子表示)
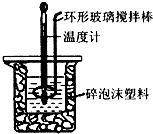
(2)用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液,在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
| 起始温度t1/℃ | 终止温度t2/℃ | 温度差 (t2-t1)/℃ | |||
| 平均值 | |||||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
②装置中大、小烧杯之间填满碎泡沫塑料的目的是减少实验过程中的热量损失;
③某同学实验记录的数据如上表所示,其中记录的终止温度是指混合溶液的最高温度;
④计算该实验发生中和反应时放出的热量为1344J[中和后生成的溶液的比热容c=4.2J•(g•℃)-1,稀溶液的密度都为1g•cm-3];
⑤若用50mL 0.55mol•L-1的氨水(NH3•H2O)代替NaOH溶液进行上述实验,通过测得的反应热来计算中和热,测得的中和热△H会偏大(填“偏大”、“偏大”或“不变”,其原因是一水合氨为弱电解质,反应过程中电离需要吸收热量,故放出的热量偏少,△H偏大.
| A. | SiO2→H2SiO3 | B. | Cu→CuSO4 | C. | Fe→FeCl2 | D. | Al→Na[Al(OH)4] |
 二氯化二硫(S2Cl2)是基本有机化工的直接原料,实验室可采用干燥的氯气在110℃-140℃与硫反应,即可得S2Cl2粗品.
二氯化二硫(S2Cl2)是基本有机化工的直接原料,实验室可采用干燥的氯气在110℃-140℃与硫反应,即可得S2Cl2粗品.(1)实验室采用如图装置制备S2Cl2:
有关物质的部分性质如表:
| 物质 | S | SCl2 | S2Cl2 |
| 熔点/℃ | 112.8 | -78 | -77 |
| 沸点/℃ | 444.6 | 59.6 | 137 |
①图中B的作用是导气和冷凝;
②装置C与D之间应增加干燥装置,原因是2S2Cl2+2H2O=3S+SO2+4HCl(用化学方程式表示)
利用改进后的正确装置进行实验,请回答下列问题:
③加热A时温度过高,会使产率偏低的原因可能是S2Cl2300℃以上完全分解、温度过高会使硫气化(填写两点)
④装置C收集到的S2Cl2粗品中可能混有的杂质有SCl2、S,为提高S2Cl2的纯度,操作时除了应控制好温度,还应注意使氧气流速平缓.
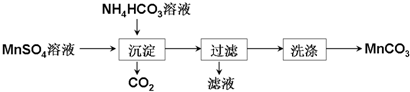
(2)工业中常用电解饱和食盐水制取2氯气,粗食盐常含有少量Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室为提纯NaCl进行以下操作:

提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液
①为除去粗食盐中的Ca2+、Mg2+、Fe3+、SO42-离子,由上述提供的试剂中选出沉淀剂a所代表的试剂,按滴加顺序依次为BaCl2、NaOH、Na2CO3(NaOH溶液的加入顺序不影响)(只填化学式)
②上述操作中操作i为溶解,操作vi为过滤;
③简述测定氯化钠中含碳酸钠质量分数的实验方案:称取样品溶解,加过量CaCl2溶液,充分反应后过滤.将沉淀洗涤干燥后称量.
| A. | 利用金属钠或者金属钾 | B. | 利用质谱法 | ||
| C. | 利用红外光谱法 | D. | 利用核磁共振氢谱 |

| A. | ①⑤ | B. | ②④ | C. | ①③⑤ | D. | ①②③⑤ |
 ;元素Z的离子结构示意图为
;元素Z的离子结构示意图为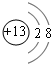 .
.