题目内容
1.现有两种烯烃:CH2═CH2和CH2═CR2(R为烃基),它们的混合物进行聚合反应,产物中可能含有( )
| A. | ①⑤ | B. | ②④ | C. | ①③⑤ | D. | ①②③⑤ |
分析 CH2═CH2和CH2═CR2混合发生加聚反应,对应产物有CH2═CH2的加聚产物、CH2═CR2的加聚产物以及CH2═CH2和CH2═CR2的加聚产物,以此解答该题.
解答 解:CH2═CH2和CH2═CR2中都双键,发生加聚反应时,可以是CH2═CH2和CH2═CH2之间发生加聚反应,可以是CH2═CR2和CH2═CR2之间发生加聚反应,也可以是CH2═CH2和CH2═CR2之间发生加聚反应;如果是CH2═CH2和CH2═CH2之间发生加聚反应生成聚乙烯就是①结构,如果是CH2═CR2和CH2═CR2之间发生加聚反应就是⑤结构,如果可以是CH2═CH2和CH2═CR2之间发生加聚反应就是②、③结构.
故选D.
点评 本题考查有机物的结构和性质,侧重考查由单体判断高聚物的结构的判断,为高频考点,难度不大,注意把握根据高聚物判断单体的方法以及单体的加聚反应产物.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.某兴趣小组模拟工业处理氨氮废水的原理,进行如下研究
(1)A中反应的化学方程式是Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑
(2)B中干燥管中应选用的药品为c(填字母)
a.无水 CuSO4 b.硅胶 c.碱石灰
(3)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)═N2(g)+6HCl(g)△H=-456kJ•mol-1
已知:

①NH3的电子式是 .
.
②断开1mol H-N键与断开1mol H-Cl键所需能量相差约为40KJkJ.
(4)现象ⅱ中产生白烟的化学方程式是HCl+NH3=NH4Cl
(5)某学生设计了如图装置以完成Cl2和NH3的反应.若该装置能实现设计目标,则
①石墨b电极上发生的是还原反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式:2NH3+6OH--6e-=N2+6H2O.
| 装置 | 操作 | 现象 |
 | 添加试剂,检查装置气密性,点燃酒精灯 | i.C中气体颜色变浅 ii.稍后,C中出现白烟并逐渐增多 |
(2)B中干燥管中应选用的药品为c(填字母)
a.无水 CuSO4 b.硅胶 c.碱石灰
(3)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)═N2(g)+6HCl(g)△H=-456kJ•mol-1
已知:

①NH3的电子式是
 .
.②断开1mol H-N键与断开1mol H-Cl键所需能量相差约为40KJkJ.
(4)现象ⅱ中产生白烟的化学方程式是HCl+NH3=NH4Cl
(5)某学生设计了如图装置以完成Cl2和NH3的反应.若该装置能实现设计目标,则

①石墨b电极上发生的是还原反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式:2NH3+6OH--6e-=N2+6H2O.
12.下列有机物的命名正确的是( )
| A. | 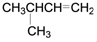 2-甲基-3-丁烯 2-甲基-3-丁烯 | B. |  1,3,4-三甲苯 1,3,4-三甲苯 | C. | 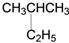 2-乙基丙烷 2-乙基丙烷 | D. | 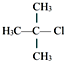 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 |
9.金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石.已知12g石墨完全转化为金刚石时,要吸收E kJ的能量,下列说法正确的是( )
| A. | 金刚石与石墨互为同分异构体 | |
| B. | 石墨转化为金刚石没有破坏化学键属于物理变化 | |
| C. | 等质量的石墨与金刚石完全燃烧,放出的能量相同 | |
| D. | 金刚石不如石墨稳定 |
6.下列说法不正确的是( )
| A. | 氢键在形成蛋白质结构和DNA双螺旋结构中起关键作用 | |
| B. | 原子光谱可用于测定物质中元素的种类 | |
| C. | 门捷列夫为元素周期律和元素周期表的发现做出了突出贡献 | |
| D. | 空气、水、煤、天然气均为可再生资源 |
10.某校学生用化学知识解决生活中的问题,下列家庭小实验中不合理的是( )
| A. | 用食醋除去暖水瓶中的薄层水垢 | |
| B. | 用米汤检验含碘盐中的碘酸钾(KIO3) | |
| C. | 用食用碱(Na2CO3)溶液洗涤餐具上的油污 | |
| D. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 |
11.一定不会加快化学反应速率的是( )
| A. | 升高温度 | B. | 增大固体的表面积 | ||
| C. | 使用催化剂 | D. | 降低溶液的温度 |