题目内容
3.由丙三醇和甲苯混合经过特殊技术可形成蒸汽组成的混合气体中,若其中混合蒸汽中碳元素的质量分数为50%,则氧元素的质量分数为( )| A. | 41.3% | B. | 8.7% | C. | 1.74% | D. | 2.14% |
分析 甲苯分子式为C7H8,甘油分子式为C3H8O3,二者相对分子质量都是92,H元素的质量分数相同,混合后H元素的质量分数不变,w(O)=1-w(C)-w(H),以此来解答.
解答 解:甲苯分子式为C7H8,甘油分子式为C3H8O3,二者相对分子质量都是92,H元素的质量分数相同为$\frac{8}{92}$×100%=8.7%,碳元素的质量分数为50%,故氧元素质量分数=1-50%-8.7%=41.3%,
故选A.
点评 本题考查元素质量分数的计算,为高频考点,把握物质的组成、元素质量分数计算方法为解答的关键,侧重分析与计算能力的考查,注意分子式及H元素的质量分数相同,题目难度不大.

练习册系列答案
相关题目
18.下列有关氯气的叙述,其说法正确的是( )


| A. | 在通常情况下氯气比空气重 | |
| B. | 点燃是使氯气和氢气化合的唯一条件 | |
| C. | 氯气跟铁反应生成FeCl2 | |
| D. | 将红热的铜放入氯气中生成蓝色氯化铜 |
15.X、Y、Z、W、R属于短周期元素,已知它们都不是稀有气体元素,X原子半径是所属周期中最大,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2:1.下列叙述中,错误的是( )
| A. | Y的最简单氢化物比R的稳定,Y的最简单氢化物沸点比R的高 | |
| B. | X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| C. | Z、W、R最高价氧化物对应水化物的酸性强弱顺序:R>W>Z | |
| D. | Y与Z两种元素组成常见ZY2型分子 |
12.除去下列物质中的杂质选用的试剂和方法最合理的是( )
| 物质 | 杂质 | 试剂 | 方法 | |
| A | 氯化铁溶液 | 氯化亚铁 | 过量铁粉 | 过滤 |
| B | 二氧化碳 | 二氧化硫 | 饱和NaHCO3溶液 | 洗气 |
| C | 二氧化硅 | 氧化铝 | 氨水 | 过滤 |
| D | 氯化钠溶液 | 碘化钠 | 四氯化碳 | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
19.氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下:
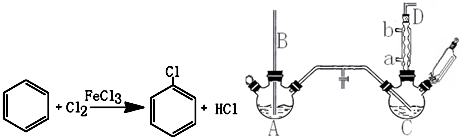
已知:氯苯为无色液体,沸点132.2℃,常温下不与氢氧化钠溶液反应.
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是平衡气压.冷凝管中冷水应从a(填“a”或“b”)处通入.
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯.
①对C加热的方法是c(填序号).
a.酒精灯加热 b.酒精喷灯加热 c.水浴加热
②D出口的气体成分有HCl、苯蒸汽和氯气.
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本.写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;HCl+NaOH=NaCl+H2O(写两个即可).
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是五氧化二磷或氯化钙.
(5)工业生产中苯的流失情况如下:
则1t苯可制得成品为$\frac{(1-0.0892)×112.5}{78}$t(只要求列式).

已知:氯苯为无色液体,沸点132.2℃,常温下不与氢氧化钠溶液反应.
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是平衡气压.冷凝管中冷水应从a(填“a”或“b”)处通入.
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯.
①对C加热的方法是c(填序号).
a.酒精灯加热 b.酒精喷灯加热 c.水浴加热
②D出口的气体成分有HCl、苯蒸汽和氯气.
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本.写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;HCl+NaOH=NaCl+H2O(写两个即可).
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是五氧化二磷或氯化钙.
(5)工业生产中苯的流失情况如下:
| 项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
| 苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
 .
. ,这种化合物中所含的化学键类型有离子键、共价键.
,这种化合物中所含的化学键类型有离子键、共价键.