题目内容
把Cl2通入NH3中恰好发生如下反应;8NH3+3Cl2═6NH4Cl+N2,反应结束时收集到84gN2,则反应有多少克NH3被氧化?
考点:氧化还原反应的计算
专题:
分析:该反应中部分N元素化合价由-3价变为0价、Cl元素化合价由0价变为-1价,根据氮原子守恒知,参加反应的氨气有
被氧化,根据参加反应的氨气和氮气之间的关系式计算.
| 1 |
| 4 |
解答:
解:此题有两种解法:
①根据8NH3+3Cl2═6NH4Cl+N2可知,氮元素的化合价升高被氧化,被氧化的氨气的质量为x
2NH3∽N2
34 28
x 84g
=
x=102g
②如果反应中有收集到84gN2,n(N2)=
=3mol,根据氮原子守恒知,被氧化的氨气的物质的量为6mol,其质量=6mol×17g/mol=102g.
答:反应有102克NH3被氧化.
①根据8NH3+3Cl2═6NH4Cl+N2可知,氮元素的化合价升高被氧化,被氧化的氨气的质量为x
2NH3∽N2
34 28
x 84g
| 34 |
| x |
| 28 |
| 84g |
x=102g
②如果反应中有收集到84gN2,n(N2)=
| 84g |
| 28g/mol |
答:反应有102克NH3被氧化.
点评:本题考查氧化还原反应的计算,明确参加反应的氨气中参加氧化还原反应的氨气的量是解本题关键,再结合原子守恒分析解答即可,题目难度不大.

练习册系列答案
相关题目
下列除杂(括号内是杂质),所用方法合理的是( )
| A、碳酸氢钠固体(碳酸钠):加热固体混合物使之分解 |
| B、铁粉(铝):加入足量稀盐酸,充分反应后过滤、洗涤、干燥 |
| C、硫酸亚铁溶液(硫酸铁):加入足量铁屑,充分反应后过滤 |
| D、二氧化碳(氯化氢):依次通过盛有氢氧化钠溶液、浓硫酸的洗气瓶 |
下列说法,不正确的是( )
| A、葡萄糖可以转变成脂肪,储存在脂肪组织中,过多食用糖类容易使人发胖 |
| B、某些植物油和鱼油中的不饱和甘油酯含量丰富,而动物脂肪中饱和甘油酯含量很高 |
| C、蛋白质溶液遇到浓的硫酸铵、硫酸钠等无机盐溶液,会析出沉淀,这个过程称为变性 |
| D、人体对维生素的需求量很小,但是,人类的生命活动不可缺少它 |
某溶液中可能含有I-、NH4+、Cu2+、SO32-、Cl-,向该溶液中加入少量溴水,振荡后溶液仍呈无色,则下列关于溶液组成的判断正确的是( )
①肯定不含I-②肯定不含Cu2+③肯定含有SO32-④可能含有I-⑤可能含有SO32-.
①肯定不含I-②肯定不含Cu2+③肯定含有SO32-④可能含有I-⑤可能含有SO32-.
| A、②④⑤ | B、①②③ |
| C、②③④ | D、①②⑤ |
下列叙述中正确的是( )
| A、乙炔能使溴的四氯化碳溶液退色,发生的是取代反应 |
| B、CH2═CH2能使酸性高锰酸钾溶液退色,发生的是氧化反应 |
| C、一氯甲烷在一定条件下即能发生水解反应也能发生消去反应 |
| D、甲苯能使酸性高锰酸钾溶液退色,说明甲苯中含碳碳双键 |
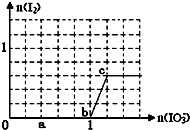 已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )
已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )| A、0~b间反应:3HSO3-+IO3-=3SO42-+I-+3H+ |
| B、a点时消耗NaHSO3的物质的量为1.2 mol |
| C、b~c间反应:I2仅是氧化产物 |
| D、c点之后碘的物质的量不变是因为还原剂消耗完全 |