题目内容
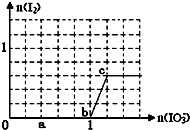 已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )
已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )| A、0~b间反应:3HSO3-+IO3-=3SO42-+I-+3H+ |
| B、a点时消耗NaHSO3的物质的量为1.2 mol |
| C、b~c间反应:I2仅是氧化产物 |
| D、c点之后碘的物质的量不变是因为还原剂消耗完全 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:还原性HSO-3>I-,所以首先是发生以下反应离子方程式:IO3-+3HSO3-═I-+3SO42-+3H+,继续加入KIO3,氧化性IO-3>I2,所以IO3-可以结合H+氧化I-生成I2,离子方程式是IO3-+6H++5I-═3H2O+3I2,根据发生的反应来判断各个点的产物.
解答:
解:还原性HSO-3>I-,所以首先是发生以下反应离子方程式:IO3-+3HSO3-═I-+3SO42-+3H+,继续加入KIO3,氧化性IO-3>I2,所以IO3-可以结合H+氧化I-生成I2,离子方程式是IO3-+6H++5I-═3H2O+3I2,
A.0~b间没有碘单质生成,说明碘酸根离子和亚硫酸氢根离子发生氧化还原反应生成碘离子,加入碘酸钾的物质的量是1mol,亚硫酸氢钠的物质的量是3mol,亚硫酸氢根被氧化生成硫酸根离子,根据转移电子守恒知,生成碘离子,所以其离子方程式为:3HSO3-+IO3-═3SO42-+I-+3H+,故A正确;
B.a点碘酸钾的物质的量是0.4mol,根据碘酸钾和亚硫酸氢钠的关系式知,消耗NaHSO3的物质的量=
×3=1.2mol,故B正确;
C.根据图象知,b-c段内发生IO3-+6H++5I-═3H2O+3I2,只有I元素的化合价变化,所以I2是氧化产物也是还原产物,故C错误;
D.碘具有氧化性,由图可知c点之后碘的物质的量不变,则是因为还原剂消耗完全,故D正确;
故选C.
A.0~b间没有碘单质生成,说明碘酸根离子和亚硫酸氢根离子发生氧化还原反应生成碘离子,加入碘酸钾的物质的量是1mol,亚硫酸氢钠的物质的量是3mol,亚硫酸氢根被氧化生成硫酸根离子,根据转移电子守恒知,生成碘离子,所以其离子方程式为:3HSO3-+IO3-═3SO42-+I-+3H+,故A正确;
B.a点碘酸钾的物质的量是0.4mol,根据碘酸钾和亚硫酸氢钠的关系式知,消耗NaHSO3的物质的量=
| 0.4mol |
| 1 |
C.根据图象知,b-c段内发生IO3-+6H++5I-═3H2O+3I2,只有I元素的化合价变化,所以I2是氧化产物也是还原产物,故C错误;
D.碘具有氧化性,由图可知c点之后碘的物质的量不变,则是因为还原剂消耗完全,故D正确;
故选C.
点评:本题考查氧化还原反应,为高频考点,明确氧化性、还原性强弱及发生反应的先后顺序是解本题关键,易错点是C,注意结合原子守恒计算,题目难度中等.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
(NH4)2Cr2O7是一种受热易分解的盐,在分解的过程中发生了氧化还原反应.下列各组对(NH4)2Cr2O7受热分解产物的判断,符合实际的是( )
| A、CrO3+NH3+H2O |
| B、Cr2O3+NH3+H2O |
| C、CrO3+N2+H2O |
| D、Cr2O3+N2+H2O |
守恒:如质量守恒,电子守恒,电荷守恒等.下列式子符合守恒思想的是( )
| A、Fe2++Cl2→Fe3++2Cl- |
| B、4FeS2+11O2→2Fe2O3+8SO2 |
| C、NH3+H2SO4→(NH4)2SO4 |
| D、Al3++6OH-→AlO2-+3H2O |
写出下列离子方程式:
(1)Na2S2O3溶液与稀硫酸反应
(2)污水中存在Cu2+加入硫化亚铁作沉淀剂
(3)浑浊的石灰水中存在的溶解平衡
(4)碳酸钠溶液呈碱性的原因
(5)泡沫灭火器的工作原理 .
(1)Na2S2O3溶液与稀硫酸反应
(2)污水中存在Cu2+加入硫化亚铁作沉淀剂
(3)浑浊的石灰水中存在的溶解平衡
(4)碳酸钠溶液呈碱性的原因
(5)泡沫灭火器的工作原理
下列化学反应属于吸热反应的是( )
| A、碘的升华 |
| B、生石灰溶于水 |
| C、氢氧化钠溶液与稀盐酸反应 |
| D、熟石灰与NH4Cl晶体混合制氨 |
 RO-CH2-OR
RO-CH2-OR