题目内容
工业上处理含Cr2O72-的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准.试回答:
(1)电解时的电极反应:阳极 ,阴极 .
(2)Cr2O72-转变成Cr3+的离子反应方程式: .
(3)常温下,Cr(OH)3的溶度积Ksp=1×10-32,溶液的pH应为 时才能使c(Cr3+)降至10-5 mol/L.
(1)电解时的电极反应:阳极
(2)Cr2O72-转变成Cr3+的离子反应方程式:
(3)常温下,Cr(OH)3的溶度积Ksp=1×10-32,溶液的pH应为
考点:电解原理
专题:电化学专题
分析:(1)在电解池中,如果阳极是活泼电极,则电极本身发生失电子的氧化反应,阴极上是阳离子发生得电子的还原反应,据此书写电极反应;
(2)Cr2O72-具有强氧化性,可以将亚铁离子氧化为铁离子,自身被还原为2Cr3+,据此书写方程式;
(3)根据溶度积常数以及水的离子积常数来进行计算.
(2)Cr2O72-具有强氧化性,可以将亚铁离子氧化为铁离子,自身被还原为2Cr3+,据此书写方程式;
(3)根据溶度积常数以及水的离子积常数来进行计算.
解答:
解:(1)用Fe为电极进行电解,阳极是活泼电极,则电极本身发生失电子的氧化反应,即Fe-2e-═Fe2+,阴极上是阳离子发生得电子的还原反应,即2H++2e-═H2↑,
故答案为:Fe-2e-═Fe2+;2H++2e-═H2↑;
(2)Cr2O72-具有强氧化性,可以将亚铁离子氧化为铁离子,自身被还原为2Cr3+,反应的实质是:6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O,
故答案为:6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O;
(3)当c(Cr3+)=10-5mol/L时,溶液的c(OH-)=
=10-9 mol/L,
c(H+)═
=10-5mol/L,pH=5,
即要使c(Cr3+)降至10-5mol/L,溶液的pH应调至5,
故答案为:5.
故答案为:Fe-2e-═Fe2+;2H++2e-═H2↑;
(2)Cr2O72-具有强氧化性,可以将亚铁离子氧化为铁离子,自身被还原为2Cr3+,反应的实质是:6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O,
故答案为:6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O;
(3)当c(Cr3+)=10-5mol/L时,溶液的c(OH-)=
| 3 |
| ||
c(H+)═
| 10 -14 |
| 10 -9 |
即要使c(Cr3+)降至10-5mol/L,溶液的pH应调至5,
故答案为:5.
点评:本题考查了电解原理、难溶物溶度积的计算、题目难度较大,涉及的知识点较多,注意掌握电解原理、难溶物溶度积的概念及计算方法,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
下列物质与其用途相符合的是( )
①Cl2-做消毒剂
②AgBr-制胶卷、感光纸
③AgI-人工降雨
④碘酸钾-制作加碘盐
⑤淀粉-检验I2的存在
⑥CaCl2-漂白纺织物.
①Cl2-做消毒剂
②AgBr-制胶卷、感光纸
③AgI-人工降雨
④碘酸钾-制作加碘盐
⑤淀粉-检验I2的存在
⑥CaCl2-漂白纺织物.
| A、②③④⑤⑥ | B、①②③④⑤ |
| C、②③④⑤ | D、全部 |
某课外实验小组设计的下列实验合理的是( )
A、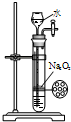 制备少量氧气 |
B、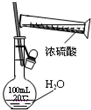 配制一定浓度硫酸溶液 |
C、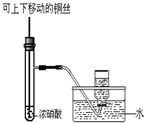 制备并收集少量NO2气体 |
D、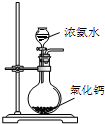 制备少量氨气 |
生活中经常用到物质分离提纯的方法,以下说法错误的是( )
| A、海水淡化是利用蒸馏的原理 |
| B、用过滤的原理使用纱布将豆腐花和豆浆分离 |
| C、酿酒时用萃取的原理将酒精的纯度提高 |
| D、海水晒盐使用了蒸发的原理 |
关于小苏打水溶液的表述正确的是( )
| A、HCO3-的电离程度大于HCO3-的水解程度 |
| B、c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| C、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| D、存在的电离有:NaHCO3=Na++HCO3-,HCO3-?H++CO32-,H2O?H++OH-,HCO3-+H2O?H2CO3+OH |
下列溶液中不能存放在带玻璃塞的试剂瓶中的是( )
①氢氟酸 ②NaCl ③KNO3 ④石灰水 ⑤CuSO4 ⑥NaOH ⑦Na2CO3 ⑧NaHSO4.
①氢氟酸 ②NaCl ③KNO3 ④石灰水 ⑤CuSO4 ⑥NaOH ⑦Na2CO3 ⑧NaHSO4.
| A、①④⑥⑦ | B、①③⑤⑧ |
| C、②③④⑦ | D、①④⑥⑧ |