题目内容
14.对下列事实的解释,错误的是( )| A. | 常温下,浓H2SO4可以用铝(或铁)容器贮存,说明浓H2SO4与Al(或Fe)常温下不反应 | |
| B. | 在蔗糖中加入浓H2SO4后出现发黑现象,说明浓H2SO4具有脱水性 | |
| C. | 浓H2SO4能使胆矾由蓝变白,说明浓H2SO4具有吸水性 | |
| D. | 稀H2SO4能与Fe反应产生H2,说明稀H2SO4也有氧化性 |
分析 A.常温下,浓硫酸与铝或铁发生钝化反应;
B.浓硫酸具有脱水性,可使蔗糖碳化;
C.浓硫酸具有吸水性,可使胆矾由蓝变白;
D.稀H2SO4能与Fe反应产生H2,H元素化合价降低.
解答 解:A.常温下,浓硫酸与铝或铁发生钝化反应,在表面生成一层致密的氧化物膜,阻碍反应的进一步进行,则常温下,浓H2SO4可以用铝(或铁)容器贮存,故A错误;
B.在蔗糖中加入浓H2SO4后出现发黑现象,说明蔗糖被碳化,可说明浓H2SO4具有脱水性,故B正确;
C.浓H2SO4能使胆矾由蓝变白,说明胆矾失去结晶水,可说明浓H2SO4具有吸水性,故C正确;
D.稀H2SO4能与Fe反应产生H2,H元素化合价降低,说明稀H2SO4也有氧化性,故D正确.
故选A.
点评 本题考查了浓硫酸的性质,明确浓硫酸的通性及特殊性质是解本题关键,浓硫酸能作干燥剂,但浓硫酸不能干燥部分还原性气体、不能干燥碱性气体,如硫化氢、氨气,为易错点.

练习册系列答案
相关题目
11.下列说法正确的是( )
| A. | 乙炔和苯均为不饱和烃,都只能发生加成反应 | |
| B. | 加新制的Cu(OH)2悬浊液并加热可检验尿液中的葡萄糖 | |
| C. | 油脂在酸的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 可以用蛋白质的焰色反应,来鉴别部分蛋白质 |
2.下列各组中两种气体所含的原子数一定相等的是( )
| A. | 温度相同,体积相同的O2和N2 | |
| B. | 质量相等,密度不等的N2和CO | |
| C. | 体积相等,密度相等的CO和C2H4 (C2H4 为乙烯气体) | |
| D. | 压强相同、体积相同的N2和O2 |
19.下列反应中,NH3既显还原性,又显碱性的是( )
| A. | NH3+HCl═NH4Cl | B. | 4NH3+5O2$\frac{\underline{\;Pt\;}}{△}$4NO+6H2O | ||
| C. | 3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O | D. | 8NH3+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$6NH4Cl+N2 |
6. 一种光化学电池的结构如图所示,电池总反应为AgCl(s)+Cu+(aq)═Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法中正确的是( )
一种光化学电池的结构如图所示,电池总反应为AgCl(s)+Cu+(aq)═Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法中正确的是( )
 一种光化学电池的结构如图所示,电池总反应为AgCl(s)+Cu+(aq)═Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法中正确的是( )
一种光化学电池的结构如图所示,电池总反应为AgCl(s)+Cu+(aq)═Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法中正确的是( )| A. | 生成108 g银,转移电子个数为1 mol | |
| B. | Cu+在负极发生氧化反应 | |
| C. | Ag电极活泼,Ag失电子发生氧化反应 | |
| D. | Cl-由负极迁移到正极 |
3.物质的量浓度相同的下列各组物质的溶液中,对指定离子的浓度作大小比较,其中错误的是( )
| A. | c(PO43-):Na3PO4>Na2HPO4>NaH2PO4>H3PO4 | |
| B. | c(CO32-):(NH4)2CO3>Na2CO3>NaHCO3>NH4HCO3 | |
| C. | c(NH4+):(NH4)2SO4>(NH4)2CO3>NH4HSO4>NH4Cl | |
| D. | c(S2-):Na2S>NaHS>H2S |
4.2SO2(g)+O2(g)═2SO3(g)的反应中,反应1分钟后,SO3的浓度增加了0.9mol/L,则O2表示的平均速率为( )
| A. | 0.45mol/(L•min) | B. | 0.55mol/(L•min) | C. | 0.60mol/(L•min) | D. | 0.90mol/(L•min) |
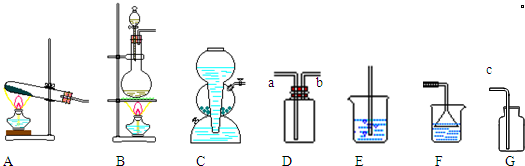
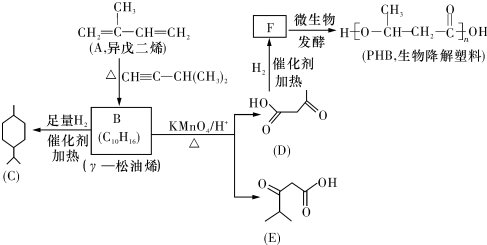
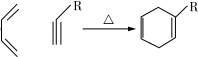
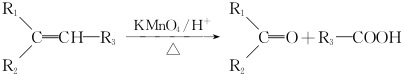
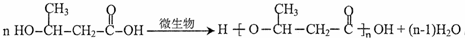 .
.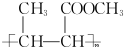 (一种类似有机玻璃的塑料).在催化剂作用下,第三步反应的化学方程式是
(一种类似有机玻璃的塑料).在催化剂作用下,第三步反应的化学方程式是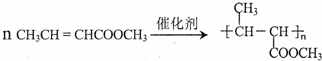 .
.