题目内容
3.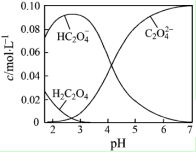 H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )| A. | pH=2.5的溶液中:c(H2C2O4)+c(C2O42-)>c(HC2O4-) | |
| B. | c(Na+)=0.100 mol•L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-) | |
| C. | c(HC2O4-)=c(C2O42-)的溶液中:c(Na+)>0.100 mol•L-1+c(HC2O4-) | |
| D. | pH=7的溶液中:c(Na+)>2c(C2O42-) |
分析 A.依据图象可知pH=2.5的溶液中:c(H2C2O4)+c(C2O42-)>c(HC2O4-);
B.依据溶液中电荷守恒和物料守恒分析,c(Na+)=0.100mol/L的溶液中c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-);
C.c(HC2O4-)=c(C2O42-)的溶液中c(Na+)<0.100 mol•L-1+c(HC2O4-);
D.20℃时,Kw=0.681×10-14,pH=7的溶液中,显酸性,(H+)>c(OH-),根据电荷守恒判断.
解答 解:A.由图象可知,pH=2.5的溶液中c(H2C2O4)和c(C2O42-)浓度之和小于c(HC2O4-),则c(H2C2O4)+c(C2O42-)>c(HC2O4-),故A错误;
B.依据溶液中电荷守恒和物料守恒分析,c(Na+)=0.100mol/L的溶液中为NaHC2O4溶液,溶液中存在电荷守恒(H+)+c(Na+)=2c(C2O42-)+c(HC2O4-)+c(OH-),物料守恒c(Na+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4),代入计算得到c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-),故B正确;
C.c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1,c(HC2O4-)=c(C2O42-),电荷守恒(H+)+c(Na+)=2c(C2O42-)+c(HC2O4-)+c(OH-),pH约4,此时氢离子浓度大于氢氧根,得到溶液中c(Na+)<0.100 mol•L-1+c(HC2O4-),故C错误;
D.20℃时,Kw=0.681×10-14,pH=7的溶液中,显酸性,(H+)>c(OH-),根据电荷守恒(H+)+c(Na+)=2c(C2O42-)+c(OH-),所以c(Na+)<2c(C2O42-),故D错误;
故选B.
点评 本题考查了弱电解质的电离、离子浓度大小比较,侧重于学生的分析能力的考查,注意把握物料守恒、电荷守恒的运用,答题时注意体会,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | SO2+2NaOH=Na2SO3+H2O | B. | SO2+Cl2+2H2O=H2SO4+2HCl | ||
| C. | SO2+2H2S=3S↓+2H2O | D. | SO2+NO2=SO3+NO |
①醋酸与水能以任意比互溶
②醋酸溶液能导电
③醋酸溶液中存在醋酸分子
④0.1mol•L-1醋酸溶液的pH比0.1mol•L-1盐酸的pH大
⑤醋酸能和碳酸钙反应放出CO2
⑥大小相同的锌粒与相同物质的量浓度的盐酸和醋酸溶液反应,开始醋酸产生H2速率慢.
| A. | ②⑥ | B. | ③④⑤⑥ | C. | ③④⑥ | D. | ①② |
| A. | 只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 | |
| B. | 将NH4Cl溶液蒸干制备NH4Cl固体 | |
| C. | 因为NH3能使酚酞溶液变红,NH3用于设计喷泉实验 | |
| D. | 浓氨水可检验氯气管道是否漏气 |
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)化学性质最不活泼的元素是Ar,其原子的原子结构示意图为
 ;
;(3)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
(4)在③~⑦元素中,原子半径最大的是Na;
(5)在 ⑦与 ⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明该事实(写出反应的化学方程式):2NaBr+Cl2=2NaCl+Br2.