题目内容
14.下列反应中,SO2被还原的是( )| A. | SO2+2NaOH=Na2SO3+H2O | B. | SO2+Cl2+2H2O=H2SO4+2HCl | ||
| C. | SO2+2H2S=3S↓+2H2O | D. | SO2+NO2=SO3+NO |
分析 SO2被还原,则S元素化合价降低,以此解答该题.
解答 解:A.S元素化合价不变,不是氧化还原反应,故A错误;
B.S元素化合价升高,二氧化硫被氧化,故B错误;
C.二氧化硫中S元素化合价由+4价降低到0价,被还原,故C正确;
D.S元素化合价升高,二氧化硫被氧化,故D错误.
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重氧化还原反应以及元素化合物知识的综合理解和运用的考查,考查学生对氧化还原反应的利用,把握反应中元素的化合价变化为解答的关键,难度不大.

练习册系列答案
相关题目
4.分类法是学习和研究化学的一种常用的科学方法,下列分类合理的是( )
| A. | 根据分散系的稳定性将其分为胶体、溶液和浊液 | |
| B. | 根据化合物在溶液中能否电离将其分为强电解质和弱电解质 | |
| C. | 根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸和多元酸 | |
| D. | 根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 |
9.下列物质的分子中,所有原子不可能都在同一平面上的是( )
| A. | 丙烯 | B. | 氯乙烯 | C. | 二氧化碳 | D. | 苯乙烯 |
19.下列化学用语表示正确的是( )
| A. | 氯化钙的化学式 CaCl2 | B. | HCl分子的电子式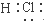 | ||
| C. | 氯化钠的电子式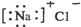 | D. | 氯原子的结构示意图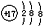 |
3.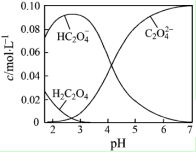 H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
 H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )| A. | pH=2.5的溶液中:c(H2C2O4)+c(C2O42-)>c(HC2O4-) | |
| B. | c(Na+)=0.100 mol•L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-) | |
| C. | c(HC2O4-)=c(C2O42-)的溶液中:c(Na+)>0.100 mol•L-1+c(HC2O4-) | |
| D. | pH=7的溶液中:c(Na+)>2c(C2O42-) |
9.漓江是我市的母亲河,保护漓江刻不容缓,下列做法中,不利于保护漓江的是( )
| A. | 将经过无害化处理的生活污水排放到漓江中 | |
| B. | 漓江沿岸不得开设造纸厂等污染企业 | |
| C. | 定期投放水生动物优化漓江生态 | |
| D. | 使用含磷洗涤剂且将洗涤后的废水排放到漓江中 |
 某实验小组设计了如图所示的甲醇燃料电池装置.
某实验小组设计了如图所示的甲醇燃料电池装置.