题目内容
11.如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
(1)从氯化钾溶液中得到氯化钾固体,选择装置D(填代表装置图的字母,下同);
分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,选择装置A ,该分离方法的名称为蒸馏.
(2)从碘水中分离出I2,选择装置B,该分离方法的名称为萃取,若将碘水和CCl4注入分液漏斗中充分振荡并静置后,碘主要溶解在下层(填“上层”或“下层”)液体中,该层溶液颜色为紫色或紫红色.
(3)装置A中①的名称是冷凝管,进水的方向是从下(填“上”或“下”)口进水.装置B在分液时为使液体顺利下滴,应进行的具体操作打开分液漏斗的上口活塞.
分析 (1)从氯化钠溶液中得到氯化钠固体,为可溶性固体与液体的分离;可用蒸馏的方法分离沸点不同的物质;
(2)碘在有机溶剂中的溶解度较大,可用萃取分液的方法分离;
(3)装置A为蒸馏操作,冷水下进上出可充分冷凝;分液时,应打开活塞和塞子.
解答 解:(1)可以采用蒸发结晶的方法从氯化钠溶液中得到氯化钠固体,则选择D装置,分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,可以采用蒸馏的方法,则选择A装置,
故答案为:D;A;蒸馏;
(2)从碘水中分离出I2,可以加入四氯化碳萃取剂,采用萃取的方法,选择B装置,碘易溶于四氯化碳,且四氯化碳的密度比水大,在水的下层,可观察到下层呈紫色或紫红色,
故答案为:B;萃取;下层;紫色或紫红色;
(3)装置A中①的名称是冷凝管,进冷却水的方向是下进上出.装置B在分液时为使液体顺利下滴,应进行的具体操作是打开分液漏斗上端活塞或使凹槽对准小孔,故答案为:冷凝管;下;打开分液漏斗的上口活塞.
点评 本题考查物质的分离提纯方法及选择,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
19.下列化学用语表示正确的是( )
| A. | 氯化钙的化学式 CaCl2 | B. | HCl分子的电子式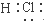 | ||
| C. | 氯化钠的电子式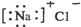 | D. | 氯原子的结构示意图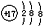 |
16.利用反应Zn+2FeCl3═ZnCl2+2FeCl2设计一个原电池.
(1)在如图图方格内画出实验装置图,
(2)指出正极材料为Pt(或石墨),电极反应式为Fe3++e-═Fe2+;负极材料为Zn,电极反应类型为氧化反应.
(3)外电路中的电子是从负(Zn)极流向正(Pt或石墨)极.
(1)在如图图方格内画出实验装置图,
(3)外电路中的电子是从负(Zn)极流向正(Pt或石墨)极.
3.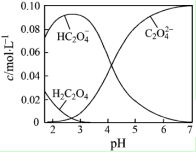 H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
 H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )| A. | pH=2.5的溶液中:c(H2C2O4)+c(C2O42-)>c(HC2O4-) | |
| B. | c(Na+)=0.100 mol•L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-) | |
| C. | c(HC2O4-)=c(C2O42-)的溶液中:c(Na+)>0.100 mol•L-1+c(HC2O4-) | |
| D. | pH=7的溶液中:c(Na+)>2c(C2O42-) |
5.2015年9月18日,美国环保署EPA宣布,大众汽车公司利用软件隐瞒了汽车有毒污染物的真实排放量,汽车尾气中的污染物有固体悬浮微粒、一氧化碳、碳氢化合物、氮氧化合物、铅及硫氧化合物等.下列有关说法中正确的是( )
| A. | 固体悬浮微粒是造成雾霾天气的一种重要因素 | |
| B. | 一氧化碳、氮氧化物是酸雨形成的主要因素 | |
| C. | 含铅化合物导致人体蛋白质变性是物理变化 | |
| D. | 汽车尾气可通过净化装置将碳氢化合物还原成CO2和H2O |
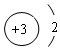 .
.