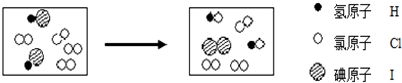
2. 某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入试剂溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀硫酸,同时打开止水夹,看到乙试管液体中有气泡冒出;再关闭止水夹,发现一段时间后乙中溶液变浑浊.符合此实验现象的一组试剂是( )
某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入试剂溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀硫酸,同时打开止水夹,看到乙试管液体中有气泡冒出;再关闭止水夹,发现一段时间后乙中溶液变浑浊.符合此实验现象的一组试剂是( )
 某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入试剂溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀硫酸,同时打开止水夹,看到乙试管液体中有气泡冒出;再关闭止水夹,发现一段时间后乙中溶液变浑浊.符合此实验现象的一组试剂是( )
某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入试剂溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀硫酸,同时打开止水夹,看到乙试管液体中有气泡冒出;再关闭止水夹,发现一段时间后乙中溶液变浑浊.符合此实验现象的一组试剂是( )| A. | KNO3 BaCl2 | B. | Na2CO3 NaOH | C. | Zn Ba(OH)2 | D. | MgCO3 Cu(NO3)2 |
15.下列物质在空气中放置一段时间后质量增加但不变质的是( )
| A. | 浓硫酸 | B. | 生石灰 | C. | 烧碱 | D. | 浓盐酸 |
14.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由不合理的猜想是猜想四,因为NaOH与H2SO4不能共存.
【继续实验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是pH试纸浸入溶液中;
(2)实验方案探究中也有一个是不合理的,不合理的原因是BaCl2和Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【实验推广1】你想过复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如硫酸和氢氧化钠反应中,实际参加反应的离子是H+和OH-,而SO42-、Na+则是“旁观者”,并没有参加反应.请你分析澄清石灰水和碳酸钠溶液反应中,参加反应的离子是Ca2+和CO32-.
【实验推广2】中和反应是没有现象的,如果要鉴别三瓶液体:稀硫酸,澄清石灰水,食盐水.提供试剂有:(A)酚酞,(B)纯碱溶液,只用一种试剂就可以将这三瓶液体区分出来,则选用试剂可以是B(从提供的试剂中选用)
0 166598 166606 166612 166616 166622 166624 166628 166634 166636 166642 166648 166652 166654 166658 166664 166666 166672 166676 166678 166682 166684 166688 166690 166692 166693 166694 166696 166697 166698 166700 166702 166706 166708 166712 166714 166718 166724 166726 166732 166736 166738 166742 166748 166754 166756 166762 166766 166768 166774 166778 166784 166792 211419
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由不合理的猜想是猜想四,因为NaOH与H2SO4不能共存.
【继续实验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 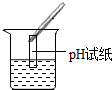 | 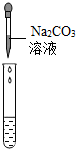 | 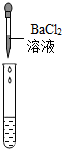 |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中只有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是pH试纸浸入溶液中;
(2)实验方案探究中也有一个是不合理的,不合理的原因是BaCl2和Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【实验推广1】你想过复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如硫酸和氢氧化钠反应中,实际参加反应的离子是H+和OH-,而SO42-、Na+则是“旁观者”,并没有参加反应.请你分析澄清石灰水和碳酸钠溶液反应中,参加反应的离子是Ca2+和CO32-.
【实验推广2】中和反应是没有现象的,如果要鉴别三瓶液体:稀硫酸,澄清石灰水,食盐水.提供试剂有:(A)酚酞,(B)纯碱溶液,只用一种试剂就可以将这三瓶液体区分出来,则选用试剂可以是B(从提供的试剂中选用)

 如图是对生成氯化钠反应关系的归纳与整理.请回答下列问题:
如图是对生成氯化钠反应关系的归纳与整理.请回答下列问题: