题目内容
14.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由不合理的猜想是猜想四,因为NaOH与H2SO4不能共存.
【继续实验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 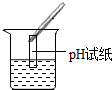 | 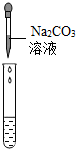 | 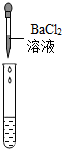 |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中只有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是pH试纸浸入溶液中;
(2)实验方案探究中也有一个是不合理的,不合理的原因是BaCl2和Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【实验推广1】你想过复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如硫酸和氢氧化钠反应中,实际参加反应的离子是H+和OH-,而SO42-、Na+则是“旁观者”,并没有参加反应.请你分析澄清石灰水和碳酸钠溶液反应中,参加反应的离子是Ca2+和CO32-.
【实验推广2】中和反应是没有现象的,如果要鉴别三瓶液体:稀硫酸,澄清石灰水,食盐水.提供试剂有:(A)酚酞,(B)纯碱溶液,只用一种试剂就可以将这三瓶液体区分出来,则选用试剂可以是B(从提供的试剂中选用)
分析 【学生板演】
氢氧化钠和稀盐酸反应生成氯化钠和水;
【假设猜想】
稀盐酸和氢氧化钠不能共存;
【继续实验】
硫酸铜能和氢氧化钠反应生成蓝色沉淀氢氧化铜和硫酸钠;
测定溶液pH的方法是:用洁净干燥的玻璃棒蘸取处理后的废水,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH;
BaCl2和Na2SO4反应会生成白色沉淀;
【实验推广1】根据复分解反应发生的条件分析作答;
【实验推广2】根据一种试剂与三种液体反应应有不同现象能区分三种液体分析作答.
解答 解:【学生板演】
氢氧化钠和稀盐酸反应生成氯化钠和水,该反应的化学方程式为:NaOH+HCl═NaCl+H2O.
故填:NaOH+HCl═NaCl+H2O.
【假设猜想】
因为氢氧化钠和稀盐酸反应生成氯化钠和水,所以氢氧化钠和稀盐酸不能共存,因此猜想四不合理.
故填:不合理的猜想是猜想四,因为NaOH与H2SO4不能共存.
【继续实验】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,说明溶液中一定没有氢氧化钠.
故填:NaOH.
【评价反思】
(1)实验操作中的错误是:把pH试纸浸入溶液中.
故填:把pH试纸浸入溶液中.
(2)实验方案中也有一个是错误的,错误的原因是BaCl2和Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
故填:BaCl2和Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【实验推广1】澄清石灰水和碳酸钠溶液反应生成碳酸钙沉淀,参加反应的离子是Ca2+和CO32-;
【实验推广2】酚酞试液滴入澄清石灰水和食盐水中均无明显变化,无法区分;纯碱溶液遇稀硫酸会有气泡产生、遇澄清石灰水会有沉淀生成,遇食盐水无明显现象,根据一种试剂与三种液体相遇有不同现象能区分三种液体;故选B.
故答案为:
【学生板演】
NaOH+HCl═NaCl+H2O.
【假设猜想】
故填:不合理的猜想是猜想四,因为NaOH与H2SO4不能共存.
【继续实验】
(1)NaOH.
【评价反思】
(1)把pH试纸浸入溶液中.
(2)BaCl2和Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【实验推广1】Ca2+;CO32-.
【实验推广2】B.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | 量筒 | B. | 胶头滴管 | C. | 天平 | D. | 玻璃棒 |
| A. | 用稀盐酸洗去水壶内的水垢 | B. | 用汽油洗去手上的油污 | ||
| C. | 用酒精洗去试管中的碘 | D. | 洗洁精洗去餐具上的油污 |
| A. | 产生了大量的热 | B. | 需要引燃 | C. | 火星四射 | D. | 生成了黑色固体 |
 如图是对生成氯化钠反应关系的归纳与整理.请回答下列问题:
如图是对生成氯化钠反应关系的归纳与整理.请回答下列问题: 如图表示一瓶氢氧化钡溶液,请按要求填写化学符号:
如图表示一瓶氢氧化钡溶液,请按要求填写化学符号: