题目内容
18.根据下列微观变化示意图回答问题.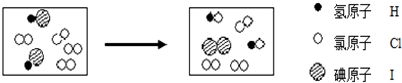
①写出表示上图微观变化的化学方程式2HI+Cl2=I2+2HCl;
②由上面的微观变化图,请你总结出化学变化的实质是分子的破裂、原子的重新组合.
分析 ①微观变化示意图分析反应物、生成物,写出变化的化学方程式;
②观察微观变化图,根据微粒的变化分析化学变化的实质.
解答 解:由微观变化示意图可知,各物质反应的微粒个数关系是:
①由微观变化示意图可知,该反应是氯气与碘化氢反应生成了氯化氢和碘,反应的方程式是:2HI+Cl2=I2+2HCl;
②由上面的微观变化图微粒的变化可知,氯分子和碘化氢分子变成了碘分子和氯化氢分子,由此可得出化学变化的实质是:分子的破裂、原子的重新组合.
故答为:①2HI+Cl2=I2+2HCl;②分子的破裂、原子的重新组合.
点评 本题主要考查了物质的微观构成和化学反应的微观示意图等方面的知识,明确每个模型表示的含义,这是解决这类题目的关键.

练习册系列答案
相关题目
14.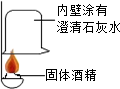 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.
【查阅资料】
(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】
(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
【实验探究】
(1)按图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论合理(选填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀与试管中加稀盐酸,有气泡产生.写出产生气体的化学方程式2NaOH+CO2═Na2CO3+H2O或CaCO3+2HCl=CaCl2+CO2↑+H2O
分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯上层清夜于两支试管中,按如图探究.
②乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是碳酸钠溶液呈碱性;也能使酚酞溶液变红.他们另取烧杯中上层清夜,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红.
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验.
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC.
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.【查阅资料】
(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】
(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
【实验探究】
(1)按图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论合理(选填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀与试管中加稀盐酸,有气泡产生.写出产生气体的化学方程式2NaOH+CO2═Na2CO3+H2O或CaCO3+2HCl=CaCl2+CO2↑+H2O
分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯上层清夜于两支试管中,按如图探究.
| 方案 | 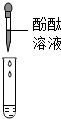 |  |
| 现象 | 溶液变红 | 产生白色沉淀 |
| 结论 | 清液有氢氧化钠 | 清液有碳酸钠 |
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验.
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC.
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
3.分类法是学习化学的重要思想方法,依据同类物质性质的相似性,可以帮助我们做到举一反三.
现有下列三组物质:
A.空气、硫酸铜、冰水、蔗糖
B.KOH、H2SO4、Ca(OH)2、Ba(OH)2
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
(2)请仿照检验CO2的反应,用SO2书写一个类似的化学反应方程式SO2+Ca(OH)2═CaSO3↓+H2O.
(3)用上述的物质写一个化学反应方程式(生成物中有二种沉淀)CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓.
现有下列三组物质:
A.空气、硫酸铜、冰水、蔗糖
B.KOH、H2SO4、Ca(OH)2、Ba(OH)2
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
| 组别 | A组 | B组 | C组 |
| 分类标准 | 纯净物 | 碱 | 盐 |
| 不属于上述分类标准的物质 | 空气 | H2SO4 | SO2 |
(3)用上述的物质写一个化学反应方程式(生成物中有二种沉淀)CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓.
10.下列实验操作中,仪器间应该接触的是( )
| A. | 做镁带燃烧实验时,夹持镁带的坩埚钳和石棉网 | |
| B. | 使用胶头滴管时,滴管尖嘴和试管内壁 | |
| C. | 向试管内直接倾倒液体时,试剂瓶口和试管口 | |
| D. | 用酒精灯加热试管时,试管底部和酒精灯灯芯 |
8.下列物质和Ba(OH)2属于不同一类物质的是( )
| A. | 熟石灰 | B. | 纯碱 | C. | 火碱 | D. | 烧碱 |
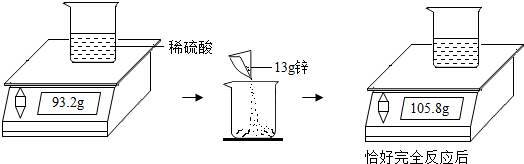

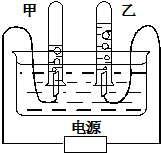 如图表示电解水的简易装置.请回答下列问题:
如图表示电解水的简易装置.请回答下列问题: