题目内容
1.实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物,极易与空气中水蒸气和CO2反应而变质.同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究.(1)【猜想】猜想Ⅰ:没有变质,“碱石灰”中只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和 Na2CO3
(2)【实验】如图所示:
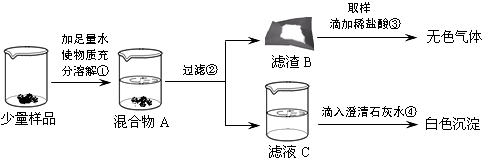
①样品实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热.
(3)【判断】
a.若Ca(OH)2、CaCO3和Na2CO3溶于水无明显的温度变化,则猜想Ⅱ不成立;(填“成立”或“不成立”)
b.操作③发生反应的化学方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O;由操作④的现象判断:滤液C中的溶质一定含有Na2CO3(写化学式);由此判断猜想Ⅰ不成立(填“成立”或“不成立”)
c.综合a和b的结论,判断该样品变质情况为部分变质(填“全部变质”或“部分变质”)
(4)【拓展】由上述实验说明,实验室中“碱石灰”应密封保存;操作②中玻璃棒的作用是引流.
分析 (3)【判断】a、根据实验中的现象结合猜想中的物质的溶于水的现象进行分析;
b、根据滤渣和滤液的成分进行分析;
c、根据流程图分析,判断哪些是肯定存在,哪些是可能;
(4)根据题中碱石灰的变化进行分析;根据操作时玻璃棒的作用进行分析.
解答 解:(3)【判断】a、Ca(OH)2、CaCO3和Na2CO3投入到水中不会放热,而样品加水溶解时试管发热,说明猜想II不成立;
b、根据题中的阳离子结合可能的变质,会生成沉淀的只有钙离子和碳酸根离子形成的碳酸钙沉淀,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,该反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;滤液中加入氢氧化钙溶液会生成白色沉淀,说明含有滤液中含有碳酸钠,进而可以判断猜想Ⅰ不成立;
c、根据上述分析可以知道该干燥剂样品中含有氧化钙、碳酸钠和碳酸钙,但是不是含有氢氧化钠在该实验过程中没有具体的验证,所以该干燥剂是部分变质;
【拓展】碱石灰在空气中极易变质,所以需要密封保存,过滤时,液体可能外溅,需要玻璃棒的引流.
故答案为:【判断】a、不成立;
b、CaCO3+2HCl═CaCl2+CO2↑+H2O;Na2CO3;不成立;
c、部分变质;
【拓展】密封;引流.
点评 在解此类题时,首先分析题中考查的知识点,然后联系学过的和题中所给的知识进行分析解答.

练习册系列答案
相关题目
17.无论是石灰水中的水,还是蒸馏水中的水,只要是水,化学式是( )
| A. | 不一样 | B. | 一样H2O | C. | 可能不一样 | D. | 不知道 |
9.下列洗涤方法中利用了乳化原理的是( )
| A. | 用稀盐酸洗去水壶内的水垢 | B. | 用汽油洗去手上的油污 | ||
| C. | 用酒精洗去试管中的碘 | D. | 洗洁精洗去餐具上的油污 |
10.如图所示制作过滤器时,滤纸的折叠方法正确的是( )


| A. | 甲→乙→丙 | B. | 甲→乙→丁 | C. | 乙→丙→丁 | D. | 甲→丙→丁 |
11.要除去氯化钠溶液中少量的碳酸钠,可加入适量的( )
| A. | 石灰水 | B. | 氯化钾溶液 | C. | 硝酸 | D. | 氯化钙溶液 |
 如图表示一瓶氢氧化钡溶液,请按要求填写化学符号:
如图表示一瓶氢氧化钡溶液,请按要求填写化学符号: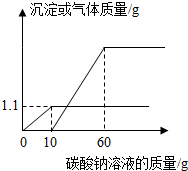 “石头纸”也叫石科纸.2010年两会期间,政协委员们领到的会议通知、日程表、便签纸等都是以碳酸钙为主要原料(假设其它物质不溶于水也不参加反应)的低碳“石头纸”.我校化学兴趣小组的同学对这种“石头纸”产生了浓厚的兴趣,进行了如下实验:
“石头纸”也叫石科纸.2010年两会期间,政协委员们领到的会议通知、日程表、便签纸等都是以碳酸钙为主要原料(假设其它物质不溶于水也不参加反应)的低碳“石头纸”.我校化学兴趣小组的同学对这种“石头纸”产生了浓厚的兴趣,进行了如下实验: