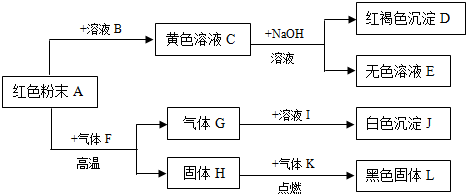
3.写出下列溶液中的溶质和溶剂
| 溶液 | 碘酒 | 98%的浓硫酸 | 石灰水 | 生理盐水 | 酒精溶液 | 盐酸 | 硫酸铜溶液 |
| 溶质 | |||||||
| 溶剂 |
2.为延缓袋装食品变质,包装时不宜采用( )
| A. | 充入氮气 | B. | 真空包装 | C. | 放人一小包铁粉 | D. | 充入氧气 |
1.请你参与某学习小组的探究活动,并回答相关问题.
【发现问题】:
(1)小雨发现盛水的铁锅在与水面接触的部位最容易生锈;
(2)小茜发现自己的铜制眼镜框表面出现了绿色的铜锈;
(3)小玲发现苹果切开后不久,果肉上会产生一层咖啡色物质,好像生了“锈”一般.
【提出问题】:这三种物质“生锈”的原因是什么?
【收集证据】:
(1)回忆已有知识;铁生锈的条件是与氧气或水接触;
(2)查阅有关资料,“铜绿”的主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成了咖啡色的物质.
(3)实验探究:将四块小铜片分别按如图所示放置一个月,观察现象如下:(提示:碱石灰可以吸收水和二氧化碳,NaOH可吸收二氧化碳)
由实验可知:铜生锈是铜与水、氧气、二氧化碳等物质共同作用的结果.
【得出结论】:经过交流谈论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与氧气(填写物质名称)有关.
【反思与应用】:
利用所得出的结论填空:
(1)写出一份防止铁或铜等金属制品生锈的具体方法保持金属表面的干净;在金属表面镀铬或镀锌;刷漆;涂油等;
(2)请你提出一条延长食品保质期的建议与氧气隔绝或充入化学性质不活泼的气体(如氮气).
【发现问题】:
(1)小雨发现盛水的铁锅在与水面接触的部位最容易生锈;
(2)小茜发现自己的铜制眼镜框表面出现了绿色的铜锈;
(3)小玲发现苹果切开后不久,果肉上会产生一层咖啡色物质,好像生了“锈”一般.
【提出问题】:这三种物质“生锈”的原因是什么?
【收集证据】:
(1)回忆已有知识;铁生锈的条件是与氧气或水接触;
(2)查阅有关资料,“铜绿”的主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成了咖啡色的物质.
(3)实验探究:将四块小铜片分别按如图所示放置一个月,观察现象如下:(提示:碱石灰可以吸收水和二氧化碳,NaOH可吸收二氧化碳)
| 实验装置 |  | 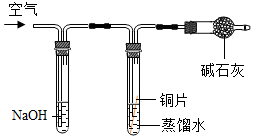 |  | 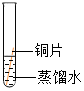 |
| 实验现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面附近锈蚀最严重 |
【得出结论】:经过交流谈论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与氧气(填写物质名称)有关.
【反思与应用】:
利用所得出的结论填空:
(1)写出一份防止铁或铜等金属制品生锈的具体方法保持金属表面的干净;在金属表面镀铬或镀锌;刷漆;涂油等;
(2)请你提出一条延长食品保质期的建议与氧气隔绝或充入化学性质不活泼的气体(如氮气).
20. 用质量相等的锌和铁分别跟质量相等、溶质的质量分数也相等的稀盐酸反应,反应情况如图所示.则下列情况不可能的是( )
用质量相等的锌和铁分别跟质量相等、溶质的质量分数也相等的稀盐酸反应,反应情况如图所示.则下列情况不可能的是( )
 用质量相等的锌和铁分别跟质量相等、溶质的质量分数也相等的稀盐酸反应,反应情况如图所示.则下列情况不可能的是( )
用质量相等的锌和铁分别跟质量相等、溶质的质量分数也相等的稀盐酸反应,反应情况如图所示.则下列情况不可能的是( )| A. | 锌、铁都反应完,盐酸有剩余 | |
| B. | 盐酸均反应完,锌、铁均有剩余 | |
| C. | 曲线a、b分别表示锌、铁的反应情况 | |
| D. | 反应完成后,两种金属产生氢气的质量相等 |
19.钢铁工业是国家工业的基础. 某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究.
[设计实验]
用一氧化碳还原纯净的氧化铁粉末,实验装置如图.
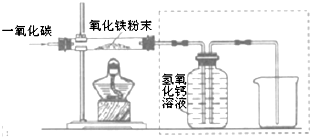
[进行实验]
该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
[分析与讨论]
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能
a.全部为铁 b.全部是四氧化三铁 c铁与四氧化三铁的混合物.
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称)四氧化三铁.
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有A、B.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
[设计实验]
用一氧化碳还原纯净的氧化铁粉末,实验装置如图.

[进行实验]
该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
| 物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能
a.全部为铁 b.全部是四氧化三铁 c铁与四氧化三铁的混合物.
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称)四氧化三铁.
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有A、B.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
17.某无色气体可能含有CO、H2、CH4中的一种或几种,依次进行以下实验(假设每步反应或吸收均完全,已知浓硫酸可吸收水,碱石灰既可以吸收水也可以吸收二氧化碳):①将气体充分燃烧,②将生成的气体通过浓硫酸,装置质量增加3.6克,③将气体通过碱石灰固体,装置质量增加4.4克.下列推断正确的是( )
| A. | 原混合气体中可能只含有CH4,也可能三种都含有 | |
| B. | 原混合气体中可能只含有H2,不含有CH4和CO | |
| C. | 原混合气体中可能只含有H2和CH4,不含有CO | |
| D. | 原混合气体中可能只含有CO和CH4,不含有H2 |
15.某硝酸铵(NH4NO3)样品(杂质不含氮)中氮元素的质量分数为28%,则该样品中硝酸铵的质量分数是( )
0 166306 166314 166320 166324 166330 166332 166336 166342 166344 166350 166356 166360 166362 166366 166372 166374 166380 166384 166386 166390 166392 166396 166398 166400 166401 166402 166404 166405 166406 166408 166410 166414 166416 166420 166422 166426 166432 166434 166440 166444 166446 166450 166456 166462 166464 166470 166474 166476 166482 166486 166492 166500 211419
| A. | 20% | B. | 35% | C. | 60% | D. | 80% |