题目内容
19.钢铁工业是国家工业的基础. 某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究.[设计实验]
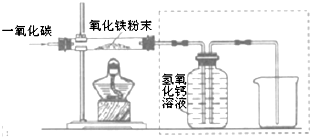
用一氧化碳还原纯净的氧化铁粉末,实验装置如图.
[进行实验]
该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
| 物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能
a.全部为铁 b.全部是四氧化三铁 c铁与四氧化三铁的混合物.
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称)四氧化三铁.
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有A、B.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
分析 【实验与猜想】
①依据表中信息找到不能被磁铁吸引的物质即可;
②由于铁与四氧化三铁均能被磁铁吸引,所以可对黑色固体进行猜测;
【得出结论】依据实验测得的数据结合氧化铁的化学式可求出氧化铁中氧的质量,再用反应前后物质的质量差与之比较判断即可;
【反思与评价】依据二氧化碳和氢氧化钠溶液的反应且一氧化碳有毒需要进行尾气处理来判断.
解答 解:【实验与猜想】
①依据表中信息可知不能被磁铁吸引的物质是氧化铁和氧化亚铁,固体全部能被吸引,说明固体中一定不含有这两者;
②由于铁与四氧化三铁均能被磁铁吸引,所以可对黑色固体的成分可能是:全部是铁;全部是四氧化三铁;两者的混合物;
【得出结论】依据实验测得的数据可知氧化铁的质量是:66g-60g=6g,这些氧化铁中含有的氧元素质量是:6g×$\frac{3×16}{2×56+3×16}$×100%=1.8g,由于反应前后固体的质量差即为氧化铁失掉的氧的质量,所以可知反应前后失掉的氧的质量是:66g-65.8g=0.2g,所以该固体不可能全是铁,固体中还有1.6g氧元素没有失掉,假设全是四氧化三铁则其含有的氧元素质量是:5.8g×$\frac{4×16}{3×56+4×16}$×100%=1.6g,故全部是四氧化三铁,所以该固体粉末是四氧化三铁;
【反思与评价】因为二氧化碳和氢氧化钠溶液能反应且无现象,一氧化碳不能与氢氧化钠反应;
A、由于一氧化碳不能与氢氧化钠反应,结合装置的特点可知该装置能收集一氧化碳,同时排出氢氧化钠溶液;
B、二氧化碳和氢氧化钠溶液能反应,所以可以用来吸收二氧化碳;
C、由于二氧化碳和氢氧化钠溶液反应时没有明显的现象产生,所以不能用它来检验二氧化碳的存在;
故答案为:【实验与猜想】①氧化亚铁;②全部是四氧化三铁;铁与四氧化三铁的混合物;
【得出结论】四氧化三铁;
【反思与评价】A、B.
点评 此题是与炼铁相关的实验探究题,综合性较强,尤其是利用数据对混合物的判断提高了试题的难度,只要是掌握固体质量变化是氧元素失掉的实质便可迎刃而解.

| A. | 它们都显电性 | |
| B. | 它们原子核外电子数目相等 | |
| C. | 它们属于同种元素 | |
| D. | 镁离子是镁原子得到2个电子形成的 |
【查阅资料】
(1)Al2O3+2NaOH=2NaAlO2+H2O;
(2)AlN+NaOH+H2O=NaAlO2+NH3↑;
(3)氨气易与酸反应.
【设计实验】
实验一:制取氮化铝样品
| 实验步骤 | 相关化学反应方程式 |
| 1除去空气中粉尘、二氧化碳、干燥后,再除去氧气. | 除去氧气的化学反应方程式为2Cu+O2$\frac{\underline{\;高温\;}}{\;}$2CuO; |
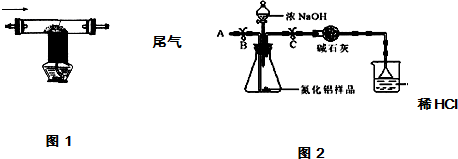
| 2用上述制得的氮气通入装有碳和三氧化二铝硬质玻璃管中高温制取氮化铝样品(如图1). | 装置中发生化学反应的化学方程式为 N2+3C+Al2O3 $\frac{\underline{\;高温\;}}{\;}$2AlN+3CO. |
①按图2组装仪器,将9.1g氮化铝样品放入锥形瓶中,在分液漏斗中加入一定量的浓NaOH溶液
②称得盛有稀盐酸的烧杯和漏斗的总质量为200g
③打开止水夹C,从分液漏斗向锥形瓶中滴入浓NaOH溶液,直到不再产生气体为止
④打开止水夹B,从导管A处缓缓鼓入一定量的空气
⑤再次称量盛有稀盐酸的烧杯和漏斗的质量和为203.4g
⑥重复实验④⑤步骤后称得盛有稀盐酸的烧杯和漏斗的总质量仍为203.4g
【实验讨论】
(1)步骤①加入样品前还应检查装置气密性.
(2)装有碱石灰的干燥管作用是除去气体中的水;装置中使用漏斗的目的是防止液体倒吸.
(3)图2烧杯中稀盐酸不能换成浓盐酸的理由是浓盐酸具有挥发性;
(4)步骤④的目的是使反应产生的氨气充分吸收.
【实验结论】
所制氮化铝样品中氮化铝的质量分数为90%
【事故处理】
实验中,小明不小心将盛有约50mL的浓NaOH溶液打翻在桌面上.这时他应该采取的措施是:立即用稀醋酸中和,然后用水冲洗,再用抹布擦干.
【拓展探究】
(1)实验后剩余的浓NaOH溶液不能(能或不能)放回原试剂瓶,写出NaOH溶液露置在空气中发生的化学反应方程式2NaOH+CO2═Na2CO3+H2O.
(2)本着节约药品的原则,同时又要确保实验顺利获得成功.则实验二中至少应准备40%浓NaOH溶液20g.
| A. | 提倡乘坐公共交通、骑自行车或步行的方式出行 | |
| B. | 在生产和生活活动中提倡使用节能技术和节能用具 | |
| C. | 植树造林,严禁乱砍滥伐 | |
| D. | 焚烧废旧塑料袋 |