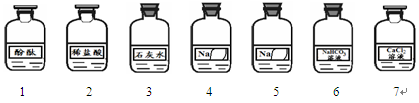
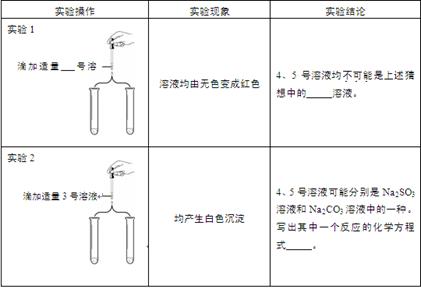
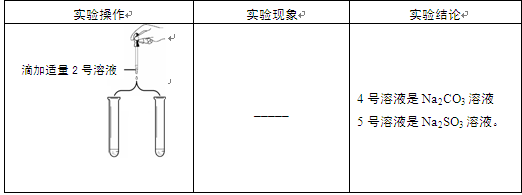
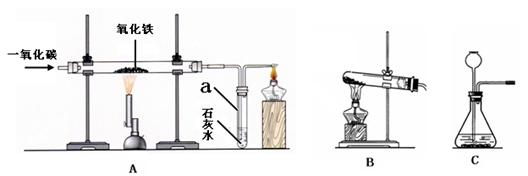
0 111372 111380 111386 111390 111396 111398 111402 111408 111410 111416 111422 111426 111428 111432 111438 111440 111446 111450 111452 111456 111458 111462 111464 111466 111467 111468 111470 111471 111472 111474 111476 111480 111482 111486 111488 111492 111498 111500 111506 111510 111512 111516 111522 111528 111530 111536 111540 111542 111548 111552 111558 111566 211419