题目内容
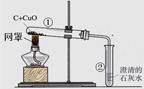
还原性铁粉在潮湿的空气中容易生锈。现有m1 g生锈的铁粉样品,某兴趣小组同学按下图所示装置进行实验,测定该样品中氧化铁的质量分数(铁锈按氧化铁处理)。

(1)装置A中反应的化学方程式是_____。
(2)某同学欲通过B装置反应前后的质量变化,测定该样品中氧化铁的质量分数。B中的最佳试剂是_____(填序号),实验时B中反应的化学方程式是_____。
① 澄清石灰水 ② 氢氧化钠浓溶液 ③ 稀盐酸 ④ 水
(3)上述实验过程中,CO气体除作为反应物外,还能起到的作用是:① 实验开始时,排尽装置中的空气,防止加热时发生爆炸;② 停止加热后,防止A中生成物被氧化,B中的溶液倒吸入A中;③_____。
(4)完全反应后,甲同学称得铁粉的质量为m2 g,同时测得装置B增重m3 g,则铁粉样品中氧化铁的质量分数为_____。

(1)装置A中反应的化学方程式是_____。
(2)某同学欲通过B装置反应前后的质量变化,测定该样品中氧化铁的质量分数。B中的最佳试剂是_____(填序号),实验时B中反应的化学方程式是_____。
① 澄清石灰水 ② 氢氧化钠浓溶液 ③ 稀盐酸 ④ 水
(3)上述实验过程中,CO气体除作为反应物外,还能起到的作用是:① 实验开始时,排尽装置中的空气,防止加热时发生爆炸;② 停止加热后,防止A中生成物被氧化,B中的溶液倒吸入A中;③_____。
(4)完全反应后,甲同学称得铁粉的质量为m2 g,同时测得装置B增重m3 g,则铁粉样品中氧化铁的质量分数为_____。
(1)3CO + Fe2O3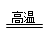 2Fe + 3CO2 (2)② CO2+2NaOH= Na2CO3 + H2O
2Fe + 3CO2 (2)② CO2+2NaOH= Na2CO3 + H2O
(3)将装置中的CO2送入NaOH溶液中。
(4)10(m1-m2) / 3m1或 40 m3/33 m1(说明:此空2分)
 2Fe + 3CO2 (2)② CO2+2NaOH= Na2CO3 + H2O
2Fe + 3CO2 (2)② CO2+2NaOH= Na2CO3 + H2O(3)将装置中的CO2送入NaOH溶液中。
(4)10(m1-m2) / 3m1或 40 m3/33 m1(说明:此空2分)
试题分析:(1)装置A中是一氧化碳还原氧化铁的反应,反应的化学方程式是3CO + Fe2O3
 2Fe + 3CO2
2Fe + 3CO2(2)某同学欲通过B装置反应前后的质量变化,测定该样品中氧化铁的质量分数,即要通过装置B来吸收A中反应生成的二氧化碳的质量,则B中的最佳试剂是②氢氧化钠浓溶液,以保证将二氧化碳全部吸收。
(3)上述实验过程中,CO气体除作为反应物外,还能起到的作用是:① 实验开始时,排尽装置中的空气,防止加热时发生爆炸;② 停止加热后,防止A中生成物被氧化,B中的溶液倒吸入A中;③将装置中的CO2送入NaOH溶液中。
(4)完全反应后,甲同学称得铁粉的质量为m2 g,同时测得装置B增重m3 g,设铁粉样品中氧化铁的质量为X。
3CO + Fe2O3
 2Fe + 3CO2
2Fe + 3CO2160 132
X m3 g
160:132=X:m3 g
X=
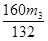 g
g铁粉样品中氧化铁的质量分数为(
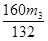 / m1)×100%=
/ m1)×100%=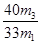
或者设样品中氧化铁的质量为Y。
则Y·
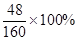 =(m1- m2)g
=(m1- m2)gY=
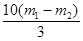 g
g铁粉样品中氧化铁的质量分数为
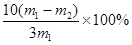 =
=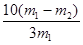
点评:书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。
一氧化碳有毒,实验中要进行尾气处理,防止一氧化碳污染空气。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目







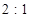 ,但自己实验所得数据氢气和氧气的体积比略大于2:1。针对这一发现,你认为下列做法中不可取的是( )
,但自己实验所得数据氢气和氧气的体积比略大于2:1。针对这一发现,你认为下列做法中不可取的是( ) 
