题目内容
1.盛放下列药品的试剂瓶,如果忘了盖瓶塞一段时间,药品不会发生变质,质量也不会发生改变的是( )| A. | 氧化钙 | B. | 碳酸钙 | C. | 酒精 | D. | 浓盐酸 |
分析 敞口瓶久置于空气发生变质即发生了化学变化,也就是与空气中的成分发生了化学反应,生成了新的物质,根据常见物质的化学性质进行分析判断.
解答 解:A、氧化钙敞口瓶久置于空气中,与空气中的水分反应生成氢氧化钙而变质,故选项错误.
B、碳酸钙不和空气中物质反应,不会发生变质,质量也不会发生改变,故选项正确.
C、酒精具有挥发性,忘了盖瓶塞一段时间,药品不会发生变质,但质量会减少,故选项错误.
D、浓盐酸具有挥发性,忘了盖瓶塞一段时间,药品不会发生变质,但质量会减少,故选项错误.
故选:B.
点评 本题难度不大,掌握常见的酸、碱、盐、生石灰的化学性质、在空气中的质量变化等是正确解答此类题的关键.

练习册系列答案
相关题目
9.白云石粉是一种生产高级玻璃器皿、医药用瓶、光学玻璃的原料,某化学兴趣小组对白云石粉极其好奇,决定对其进行探究.
【查阅资料】白云石属于碳酸盐矿物,白云石粉主要成分的化学式可表示为:xMgCO3•yCaCO3.( 杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一.定性探究:白云石粉的成分和性质

【实验分析】
(1)过滤操作中用到的玻璃仪器有玻璃棒、烧杯、漏斗.
(2)由步骤①②的现象可得出白云石粉中一定含有的离子是CO32-(填离子符号).
(3)步骤③生成氢氧化镁的化学方程式是MgCl2+2NaOH═Mg(OH)2↓+2NaCl.步骤④的反应现象是产生白色沉淀.
【结论】综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成.
[实验质疑】小组同学经过讨论认为:因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究.
二.定量探究:白云石的组成
[查阅资料】碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸钙与碳酸镁的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解.
【实验设计】为测定白云石中的含钙量及x:y的值,该兴趣小组设计了如下装置并进行实验:

【实验步骤】①组装仪器,检查装置的气密性;②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D装置的质量;③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量;⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量.
实验数据记录如表:
【实验分析和数据处理】
(4)装置D的作用是吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小;
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是使残留在装置内的二氧化碳气体全部被C装置吸收.
(6)计算白云石中钙元素的质量分数.(写出计算过程,结果保留小数点后一位):
(7)设计实验证明白云石粉已完全分解的实验方法是取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解(写出实验方法、现象、结论)
(8)白云石(xMgCO3•yCaCO3)中的 x:y=1:2(最简整数比),若加热前没有鼓入一段时间的氮气,将会导致x:y的值偏大(填偏大、偏小或不变).
【查阅资料】白云石属于碳酸盐矿物,白云石粉主要成分的化学式可表示为:xMgCO3•yCaCO3.( 杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一.定性探究:白云石粉的成分和性质

【实验分析】
(1)过滤操作中用到的玻璃仪器有玻璃棒、烧杯、漏斗.
(2)由步骤①②的现象可得出白云石粉中一定含有的离子是CO32-(填离子符号).
(3)步骤③生成氢氧化镁的化学方程式是MgCl2+2NaOH═Mg(OH)2↓+2NaCl.步骤④的反应现象是产生白色沉淀.
【结论】综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成.
[实验质疑】小组同学经过讨论认为:因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究.
二.定量探究:白云石的组成
[查阅资料】碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸钙与碳酸镁的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解.
【实验设计】为测定白云石中的含钙量及x:y的值,该兴趣小组设计了如下装置并进行实验:

【实验步骤】①组装仪器,检查装置的气密性;②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D装置的质量;③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量;⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量.
实验数据记录如表:
| B中溶液质量/g | C中溶液质量/g | D中溶液质量/g | |
| 反应前 | 50.0 | 100.0 | 50.0 |
| 700℃ | 50.0 | 102.1 | 50.1 |
| 1000℃ | 50.0 | 106.3 | 50.3 |
(4)装置D的作用是吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小;
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是使残留在装置内的二氧化碳气体全部被C装置吸收.
(6)计算白云石中钙元素的质量分数.(写出计算过程,结果保留小数点后一位):
(7)设计实验证明白云石粉已完全分解的实验方法是取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解(写出实验方法、现象、结论)
(8)白云石(xMgCO3•yCaCO3)中的 x:y=1:2(最简整数比),若加热前没有鼓入一段时间的氮气,将会导致x:y的值偏大(填偏大、偏小或不变).
16.柠檬酸(其化学式为C6H8O7)是一种重要的有机酸,它在工业、食品业、化妆业等具有极多的用途.下列有关柠檬酸的说法中错误的是( )
| A. | 柠檬酸是由碳、氢、氧三种元素组成的 | |
| B. | 柠檬酸的相对分子质量为192 | |
| C. | 一个柠檬酸分子中含有6个碳原子、8个氢原子和7个氧原子 | |
| D. | 柠檬酸中,碳、氢、氧三种元素的质量比为6:8:7 |
10.如图是硝酸钾和氯化钠两种固体物质的溶解度曲线,下列叙述错误的是( )

| A. | t1℃时,向分别盛有3.6g NaCl和KMO3固体的烧杯中各加入10g水,充分搅拌后两种固体能全部溶解 | |
| B. | t2℃时,NaCl和KMO3两种物质的饱和溶液都降温至t1℃,两种溶液中溶质的质量分数相等 | |
| C. | t2℃时,将100g KMO3饱和溶液降温到t1℃,会有44g晶体析出 | |
| D. | KMO3中含有少量NaCl,可以用冷却热饱和溶液的方法提纯KMO3 |
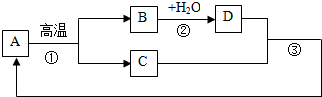
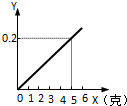 某不纯的铁粉与稀硫酸反应时,质量关系如图所示,x表示不纯铁粉消耗的质量,Y表示生成氢气的质量,试判断不纯铁粉中混入的杂质是( )
某不纯的铁粉与稀硫酸反应时,质量关系如图所示,x表示不纯铁粉消耗的质量,Y表示生成氢气的质量,试判断不纯铁粉中混入的杂质是( )