题目内容
10.某研究性学习小组设计了测定纯碱样品(只含NaCl杂质)中碳酸钠质量分数的实验方案.请回答下列问题:(1)碳酸根离子沉淀法.实验步骤:
①用托盘天平称取样品wg放入烧杯中加水溶解;
②加入足量BaCl2溶液充分反应.证明反应后BaCl2剩余的方法是静置,取少量上层清液,加入少量碳酸钠溶液,有白色沉淀生成,证明氯化钡剩余;
③过滤、洗涤、干燥、称量沉淀的质量为mg;
④计算出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
(2)指示剂变色法.实验步骤:
①用托盘天平称取样品10.6g放入烧杯中加水溶解;
②滴入几滴酚酞溶液;
③用滴管慢慢滴入10%的稀盐酸,并不断搅拌,至溶液颜色恰好变为无色为止,共用去了稀盐酸7.3g.请回答:
a.酚酞溶液的作用是判断是否恰好完全反应;
b.边滴加稀盐酸,边要用玻璃棒不断搅拌的目的是使反应物充分接触,完全反应.
c.反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑,10.6g样品中含碳酸钠的质量为1.06g,样品中碳酸钠质量分数为10%(用百分数表示).
(3)测氯化钠法.请你完成下列实验方案:
①取一些样品放入烧杯中加水溶解:
②加入足量稀硝酸,再加入足量的硝酸银溶液;加入硝酸银溶液时发生反应的化学方程式是:AgNO3+NaCl═AgCl↓+NaNO3.
③过滤、洗涤、干燥、称量沉淀的质量为mg;
④计算出氯化钠的质量,再求样品中碳酸钠的质量分数.但实验后有同学发现,按上述操作步骤是不能计算出碳酸钠的质量分数,原因是开始没有称量样品的质量.
分析 根据氯化钡能与碳酸钠反应生成碳酸钡沉淀分析解答;酚酞试液在碱性溶液中变红;玻璃棒搅拌能促进物质间的接触,加快反应的进行;碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳;根据盐酸的质量求碳酸钠的质量,进而求算碳酸钠的质量分数;硝酸银能与氯化钠反应生成氯化银沉淀和硝酸钠,据此解答.
解答 解:(1)②氯化钡能与碳酸钠反应生成碳酸钡沉淀,故可以加入碳酸钠溶液观察是否产生白色沉淀的方法证明氯化钡的剩余,故填:静置,取少量上层清液,加入少量碳酸钠溶液,有白色沉淀生成,证明氯化钡剩余;
(2)③a、根据酚酞试液颜色的变化判断反应是否恰好完全进行,故填:判断是否恰好完全反应;
b、玻璃棒搅拌能促进物质间的接触,加快反应的进行,故填:使反应物充分接触,完全反应;
c、碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,设碳酸钠的质量为x,则有
Na2CO3+2HCl═2NaCl+H2O+CO2↑;
106 73
x 7.3g×10%
$\frac{106}{73}=\frac{x}{7.3g×10%}$
x=1.06g
故碳酸钠的质量分数为:$\frac{1.06g}{10.6g}×100%$=10%;
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑,1.06g,10%;
(3)②硝酸银能与氯化钠反应生成氯化银沉淀和硝酸钠,故填:AgNO3+NaCl═AgCl↓+NaNO3;
④取一些样品并没有称量,故无法进行计算,故填:开始没有称量样品的质量.
点评 本题考查的是混合物成分及其含量的实验探究,完成此题,可以依据已有的物质的性质结合题干提供的信息进行.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
20.小刚同学根据所学化学知识,向家人提出了如下建议,其中不合理的是( )
| A. | 霉变的大米蒸熟后食用无害 | B. | 用灼烧的方法能鉴别绦纶和羊毛 | ||
| C. | 用食醋除去水壶中的水垢 | D. | 用加热煮沸的方法降低水的硬度 |
5. 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃,实验时打开导管中的开关.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃,实验时打开导管中的开关.
(1)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,燃烧匙中白磷不燃烧的原因是未达到白磷的着火点; 烧杯中白磷未燃烧的原因是白磷没有与O2接触; 推入H2O2溶液后,观察到烧杯中的现象是导管口有气泡冒出,烧杯中的白磷燃烧.
(2)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是助燃;木炭熄灭后冷却一段时间,烧杯中的溶液能(填“能”或“否”)流入集气瓶.
 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃,实验时打开导管中的开关.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃,实验时打开导管中的开关.| 内容 步骤 | 【实验1】研究燃烧条件 | 【实验2】研究氧气性质 |
| Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和 烧杯中导管口放置一 小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2 溶液 | 推入适量H2O2 溶液 |
(2)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是助燃;木炭熄灭后冷却一段时间,烧杯中的溶液能(填“能”或“否”)流入集气瓶.
15.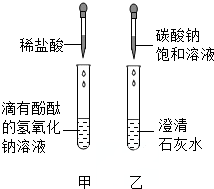 同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.
同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.
(1)写出甲实验的化学反应方程式HCl+NaOH=NaCl+H2O.
(2)实验结束后,甲、乙两个同学将废液倒入实验室的废液缸中,结果发现废液浑浊并呈红色,于是他们产生了疑问.
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、NaCl和水.
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小刚认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是NaOH.(写一种猜想)
【设计实验】小芳想用氯化钙溶液来验证小刚、小红、小林的猜想.查阅资料得知氯化钙溶液呈中性,并设计如下实验.请你将小芳的实验设计补充完整.
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑反应物的用量.
 同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.
同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.(1)写出甲实验的化学反应方程式HCl+NaOH=NaCl+H2O.
(2)实验结束后,甲、乙两个同学将废液倒入实验室的废液缸中,结果发现废液浑浊并呈红色,于是他们产生了疑问.
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、NaCl和水.
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小刚认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是NaOH.(写一种猜想)
【设计实验】小芳想用氯化钙溶液来验证小刚、小红、小林的猜想.查阅资料得知氯化钙溶液呈中性,并设计如下实验.请你将小芳的实验设计补充完整.
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管 中,加入过量氯化钙溶液,静置. | ①有白色沉淀,溶液呈红色. | 小林的猜想正确. |
| ②产生白色沉淀、溶液为无色. | 小刚的猜想正确. | |
| ③无白色沉淀,溶液呈红色. | 小红的猜想正确. |
2.草木灰的主要成分是碳酸钾(K2CO3),下列关于草木灰的说法中错误的是( )
| A. | 可作钾肥 | B. | 由三种元素组成 | ||
| C. | K2CO3属于盐类 | D. | 碳元素的化合价是+2价 |
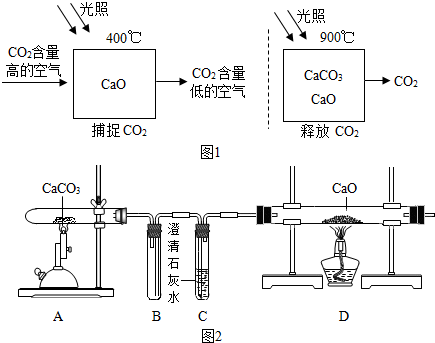
 金属材料与人类的生产和生活密切相关.
金属材料与人类的生产和生活密切相关.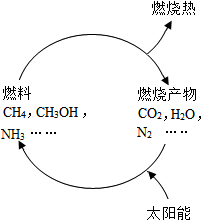 (1)从能源是否可以循环再生的角度看,可以将能源分为可再生能源和不可再生能源,譬如煤、石油、天然气就是不可再生能源.日益严峻的能源危机促进了可再生能源的研究.有专家提出:如果能够利用太阳能使燃料燃烧产物,如CO2、H2O、N2等重新组合(如图),可以节约燃料,缓解能源危机.在此构想的物质循环中太阳能最终转化为热能.
(1)从能源是否可以循环再生的角度看,可以将能源分为可再生能源和不可再生能源,譬如煤、石油、天然气就是不可再生能源.日益严峻的能源危机促进了可再生能源的研究.有专家提出:如果能够利用太阳能使燃料燃烧产物,如CO2、H2O、N2等重新组合(如图),可以节约燃料,缓解能源危机.在此构想的物质循环中太阳能最终转化为热能.