题目内容
2.草木灰的主要成分是碳酸钾(K2CO3),下列关于草木灰的说法中错误的是( )| A. | 可作钾肥 | B. | 由三种元素组成 | ||
| C. | K2CO3属于盐类 | D. | 碳元素的化合价是+2价 |
分析 A、根据钾肥是指含有钾元素的肥料;B、根据化学式中元素组成考虑;C、根据盐是指电离出金属离子和酸根离子的化合物;D、根据元素化合价的计算方法考虑.
解答 解:A、K2CO3中含有钾元素,属于钾肥,故A说法正确;
B、K2CO3中含有三种元素,故B说法正确;
C、盐是指电离出金属离子和酸根离子的化合物,所以K2CO3属于盐类,故C说法正确;
D、根据正负化合价代数和为零,计算出K2CO3中碳元素化合价是+4价,故D说法错误.
故选D.
点评 解答本题关键是要知道酸碱盐的分类,化学肥料的判断方法,在化合物中正负化合价代数和为零计算未知元素的化合价.

练习册系列答案
相关题目
12.下列关于物质用途的说法,错误的是( )
| A. | 用金刚石钻探机的钻头 | |
| B. | 用小苏打作焙制糕点的发酵粉 | |
| C. | 用甲醛浸泡海鲜防止其变质 | |
| D. | 用含氢氧化镁的药物治疗胃酸过多症 |
17.下列归类错误的是( )
| 选项 | 归类 | 物质(或元素) |
| A | 常见合金 | 黄铜、硬铝、青铜 |
| B | 常见的干燥剂 | 浓硫酸、生石灰、碱石灰 |
| C | 常见复合材料 | 钢筋混凝土、聚乙烯塑料、玻璃钢 |
| D | 人体中常见微量元素 | 碘、锌、硒、铁等 |
| A. | A | B. | B | C. | C | D. | D |
14.下列实验操作中,正确的是( )
| A. | 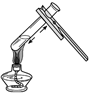 | B. |  | C. | 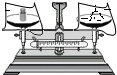 | D. | 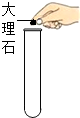 |
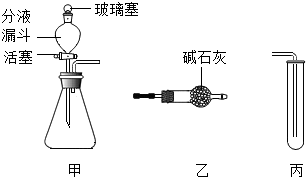 将图所示甲、乙、丙装置进行不同的组合,可以完成不同的实验,其中涉及的物质为初中化学常见物质.(提示:碱石灰的主要成分是CaO和NaOH)
将图所示甲、乙、丙装置进行不同的组合,可以完成不同的实验,其中涉及的物质为初中化学常见物质.(提示:碱石灰的主要成分是CaO和NaOH) 甲、乙两个化学兴趣小组的同学为测定某地石灰石的质量分数(杂质不参与反应),分别设计方案并进行实验.
甲、乙两个化学兴趣小组的同学为测定某地石灰石的质量分数(杂质不参与反应),分别设计方案并进行实验.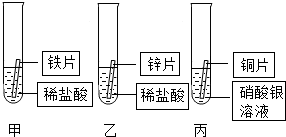 某研究小组的同学为探究铁、铜、锌、银的金属活动性顺序,设计如图所示的三个实验(其中金属均已用砂纸打磨,且形状、大小相同;所用稀盐酸的溶质质量分数、用量也相同).
某研究小组的同学为探究铁、铜、锌、银的金属活动性顺序,设计如图所示的三个实验(其中金属均已用砂纸打磨,且形状、大小相同;所用稀盐酸的溶质质量分数、用量也相同).