题目内容
20.小刚同学根据所学化学知识,向家人提出了如下建议,其中不合理的是( )| A. | 霉变的大米蒸熟后食用无害 | B. | 用灼烧的方法能鉴别绦纶和羊毛 | ||
| C. | 用食醋除去水壶中的水垢 | D. | 用加热煮沸的方法降低水的硬度 |
分析 A、根据霉变的大米中含有黄曲霉毒素进行分析判断.
B、羊毛的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味.
C、根据水垢的主要成分是碳酸钙,进行分析判断.
D、根据降低水的硬度的方法进行分析判断.
解答 解:A、霉变的大米中含有有毒的黄曲霉毒素,即使洗净蒸熟后也不能食用,故选项说法错误.
B、羊毛的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味,绦纶燃烧会产生特殊气味,可以鉴别,故选项说法正确.
C、水垢的主要成分是碳酸钙,能与食醋中的醋酸反应生成易溶于水的醋酸钙,可除去水瓶胆中的水垢,故选项说法正确.
D、生活中可用加热煮沸的方法降低水的硬度,故选项说法正确.
故选:A.
点评 与人类生产生活相关的化学知识是中考的热点,了解生活中常见的有毒物质(甲醛、黄曲霉素等)、羊毛与合成纤维的鉴别方法、碳酸钙的化学性质、硬水软化的方法是正确解答本题的关键.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 10mL酒精和10mL水混合后体积小于20mL,说明分子的质量很小 | |
| B. | 核外电子数相同的微粒一定属于同种元素 | |
| C. | 挖空沼气池前先进行火把实验 | |
| D. | 同种元素组成的物质,性质不一定相同 |
11.在化学反应前后,肯定不会发生变化的是( )
①分子的数目 ②元素的种类 ③原子的数目 ④物质的种类 ⑤物质的质量总和.
①分子的数目 ②元素的种类 ③原子的数目 ④物质的种类 ⑤物质的质量总和.
| A. | ①②③④ | B. | ①③⑤ | C. | ②③⑤ | D. | ①③④⑤ |
15.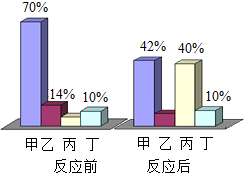 在一定条件下,甲、乙、丙、丁在某密闭容器中发生反应,测得反应前后各物质的质量分数如图所示.不正确的说法是( )
在一定条件下,甲、乙、丙、丁在某密闭容器中发生反应,测得反应前后各物质的质量分数如图所示.不正确的说法是( )
 在一定条件下,甲、乙、丙、丁在某密闭容器中发生反应,测得反应前后各物质的质量分数如图所示.不正确的说法是( )
在一定条件下,甲、乙、丙、丁在某密闭容器中发生反应,测得反应前后各物质的质量分数如图所示.不正确的说法是( )| A. | 该反应是化合反应 | |
| B. | 若消耗3g乙,则生成17g丙 | |
| C. | 丁可能是该反应的催化剂 | |
| D. | 甲、乙的质量之和一定等于生成丙的质量 |
12.下列关于物质用途的说法,错误的是( )
| A. | 用金刚石钻探机的钻头 | |
| B. | 用小苏打作焙制糕点的发酵粉 | |
| C. | 用甲醛浸泡海鲜防止其变质 | |
| D. | 用含氢氧化镁的药物治疗胃酸过多症 |
9.化学兴趣小组的同学利用废铜制取硫酸铜,设计了如下两个方案,
方案一:Cu$→_{△}^{o_{2}}$CuO$\stackrel{稀硫酸}{→}$CuSO4
方案二:Cu$→_{△}^{浓硫酸}$CuSO4[Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O]
下列说法正确的是( )
方案一:Cu$→_{△}^{o_{2}}$CuO$\stackrel{稀硫酸}{→}$CuSO4
方案二:Cu$→_{△}^{浓硫酸}$CuSO4[Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O]
下列说法正确的是( )
| A. | 方案一节约能源 | B. | 方案二铜的利用率较低 | ||
| C. | 方案一不产生污染大气的二氧化硫 | D. | 方案二硫酸的利用率较低 |
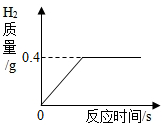 现有一块质量为20克的铜锌合金,将它投入到100克稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示,试计算:
现有一块质量为20克的铜锌合金,将它投入到100克稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示,试计算: