题目内容
3.某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:①称取mg胆矾晶体,研细后加入蒸馏水全部溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按表中的质量混合好固体,在相同条件下加热,进行比较,其它可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 加入物质质量(g) | 待测数据 |
| 1 | 2.0 | CuO x | |
| 2 | 2.0 | MnO2 0.5 |
(1)请写出上述实验步骤③中涉及到的化学方程式:Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O
(2)表格中的“待测数据”是指生成一定量气体所需时间.
(3)为使本实验具有说服力,在本实验中CuO的质量应取x=0.5g.
(4)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.(提示:可从催化剂的概念完成实验.)
| 实验步骤 | 设计这一步骤的目的 |
| 实验表明,加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
| 将加热后残留的固体溶于足量的水,过滤后称重CuO的质量 | CuO的质量在反应前后是否保持不变 |
| 将过滤后的CuO重新与KClO3混合加热,观察是否依旧能加快KClO3的分解(或者利用CuO的常见化学性质如:将CuO加入稀硫酸中,观察无色溶液是否变成蓝色) | CuO的化学性质在反应前后是否保持不变 |
分析 (1)根据氢氧化铜受热时能分解成氧化铜和水分析;
(2)实验的目的是:证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较,上述实验中已有数据KClO3质量和其它物质质量,要比较催化效果就是看使用氧化铜与二氧化锰哪一种产生相同体积气体时所需时间短,或在相同时间内,哪一种物质产生的气体多.
(3)根据加入二氧化锰的质量分析回答;
(4)根据催化剂的特点分析验证的方法.
解答 解:(1)由题意可知,在步骤③中氢氧化铜受热时能分解成氧化铜和水,涉及到的化学方程式:Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O
(2)证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较,对比实验一定要控制变量,此实验中应控制氯酸钾质量、气体的体积、氧化铜与二氧化锰的质量相等,可变的量是生成等体积(50mL)气体所需用的时间.
(3)由于二氧化锰的质量为0.5g,为使本实验具有说服力,在本实验中CuO的质量应取x=0.5g.
(4)因为催化剂的特点是:能改变其它物质的化学反应速率,但它本身的质量和化学性质在反应前后不变,所以还应该做的实验如下表:
| 实验步骤 | 实验操作及现象 | 设计目的 |
| 1 | 实验表明,加入CuO后产生O2的速率比未加时快得多 | CuO能加快KClO3的分解 |
| 2 | 将加热后残留的固体溶于足量的水,过滤后称重CuO的质量 | CuO的质量在反应前后是否保持不变 |
| 3 | 将过滤后的CuO重新与KClO3混合加热,观察是否依旧能加快KClO3的分解(或者利用CuO的常见化学性质如:将CuO加入稀硫酸中,观察无色溶液是否变成蓝色) | CuO的化学性质在反应前后是否保持不变 |
| 实验步骤 | 设计这一步骤的目的 |
| 将过滤后的CuO重新与KClO3混合加热,观察是否依旧能加快KClO3的分解(或者利用CuO的常见化学性质如:将CuO加入稀硫酸中,观察无色溶液是否变成蓝色) | CuO的化学性质在反应前后是否保持不变 |
点评 本题属于实验探究题,同学需要根据题意并结合课本所学相关知识深入分析,这类题有些答案并不固定但必须合理.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.(1)“碘是智慧元素”,它是合成甲状腺激素的重要原料之一,若人在幼年时期甲状腺激素分泌不足,可能会患C. A.白内障 B.贫血症 C.呆小症 D.夜盲症
(2)我国大部分地区缺碘,早在上世纪90年代就颁布了《食盐加碘消除碘缺乏危害管理条例》,食盐加碘成为一项国家政策.“加碘盐”一般是在食盐中加入一定量的碘酸钾(KIO3),碘酸钾属于B.
A.混合物 B.化合物 C.氧化物 D.单质
(3)表为某品牌食盐的产品说明,其中“含碘量 (35±15)mg/kg”表示在1kg“加碘盐”中含碘元素(35±15)mg,符合国家食盐含碘量的标准.若以含碘量35mg/kg为标准,食盐厂家应该在1kg食盐中加入59mg碘酸钾.(取整数)
(4)“碘是一把双刃剑”,碘过量也会引起甲状腺疾病.初中生每天碘元素适宜摄入量约为0.15mg,假设碘元素全部来自“加碘盐”,你一天最多可以摄入含碘量为35mg/kg的食盐4.3g.(保留一位小数)
(2)我国大部分地区缺碘,早在上世纪90年代就颁布了《食盐加碘消除碘缺乏危害管理条例》,食盐加碘成为一项国家政策.“加碘盐”一般是在食盐中加入一定量的碘酸钾(KIO3),碘酸钾属于B.
A.混合物 B.化合物 C.氧化物 D.单质
(3)表为某品牌食盐的产品说明,其中“含碘量 (35±15)mg/kg”表示在1kg“加碘盐”中含碘元素(35±15)mg,符合国家食盐含碘量的标准.若以含碘量35mg/kg为标准,食盐厂家应该在1kg食盐中加入59mg碘酸钾.(取整数)
| 产品标准号: | GB5461-2000 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 质量等级 | 一级 |
| 碘含量 | 35±15mg/kg |
| 食用方法 | 待食品熟后加入碘盐 |
| 储藏方法 | 密封储存、防潮加热 |
| 分装日期 |
18.逻辑推理是化学学习中常用的思维方法,以下推理正确的是( )
| A. | 化合物都是由不同种元素组成的,不同元素组成的纯净物一定是化合物 | |
| B. | 碱中都有氢、氧元素,所以含氢、氧元素的化合物都是碱 | |
| C. | 中和反应有盐和水生成,生成盐和水的反应都属于中和反应 | |
| D. | 氧化物中一定含有氧元素,则另一种元素一定是金属元素 |
8.按照一定的依据把物质进行分类,是我们认识物质的组成、结构、性质和用途的便捷途径.小明同学在家中建立了小小化学实验室,他收集了许多物质,其中有:①纯碱;②生石灰;③酒精;④熟石灰;⑤尿素CO(NH2)2;⑥铜;⑦石墨;⑧氧化铁.⑨冰醋酸.对上述物质的分类不正确的是( )
| A. | 属于有机物的有③⑤⑨ | B. | 属于碱的有①④ | ||
| C. | 属于氧化物的有②⑧ | D. | 属于单质的有⑥⑦ |
15.下列各组的两个变化都属于化学变化的是( )
| A. | 酒精的挥发;酒精的燃烧 | B. | 电解水;点燃氢气 | ||
| C. | 硝酸钾加热熔化;水结冰 | D. | 工业制氧气;实验室制氧气 |
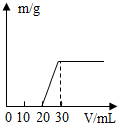 某澄清溶液由HNO3、Na2SO4、K2CO3、CuCl2 四种物质中的两种组成,向溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量(m)与加入Ba(OH)2溶液的体积(V)的关系如图所示.则该溶液所含的溶质是HNO3、CuCl2.(填化学式)
某澄清溶液由HNO3、Na2SO4、K2CO3、CuCl2 四种物质中的两种组成,向溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量(m)与加入Ba(OH)2溶液的体积(V)的关系如图所示.则该溶液所含的溶质是HNO3、CuCl2.(填化学式)