题目内容
15. 氢氧化钠曝录在空气中能与二氧化碳反应变质,写出反应的化学方程式CO2+2NaOH═Na2CO3+H2O.
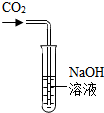
氢氧化钠曝录在空气中能与二氧化碳反应变质,写出反应的化学方程式CO2+2NaOH═Na2CO3+H2O.学习小组的同学们将二氧化碳通入盛有氢氧化钠溶液的大试管中,探究二氧化碳能否与氢氧化钠溶液反应,如图所示.结果同学们没有观察到明显现象,于是他们展开了如下探究.
探究一:二氧化碳是否与氢氧化钠发生了化学反应?
【实验过程】
甲同学们取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到产生气泡,证明二氧化碳与氢氧化钠发生了反应.
乙同学取少量大试管中的液体于另一支试管中,滴加酚酞溶液,观察到溶液变红,证明二氧化碳与氢氧化钠没有发生反应.
【交流讨论】同学们一直认为甲同学的实验及结论正确,而乙同学是错误的,乙同学错误的理由是不能滴加酚酞试液,氢氧化钠溶液和碳酸钠溶液均显碱性,能使酚酞试液变红色
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】同学们认为有两种可能:一是碳酸钠;二是碳酸钠和氢氧化钠.
【查阅资料】CaCl2溶液呈中性.
【实验验证】为了验证上述猜想哪一个是正确,甲同学设计如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量大试管中的溶液于试管,加入足量CaCl2溶液,过滤 ②向滤液滴加适量无色酚酞试液 | 产生白色沉淀,溶液呈无色 | 猜想一正确 |
| 产生白色沉淀,溶液呈红色 | 猜想二正确 |
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可;
【交流讨论】碳酸钠溶液与氢氧化钠溶液均显碱性,能使无色的酚酞试液变红色;
【提出猜想】氢氧化钠可能完全参与反应,也可能部分参与反应;
【实验验证】滴加氯化钙溶液来检验是否生成了碳酸钠,反应完全后滴加无色的酚酞试液检验是否含有氢氧化钠;
【实验反思】滴加足量的氯化钡溶液是为了使得碳酸钠完全参与反应.
解答 解:氢氧化钠应密封保存,因为氢氧化钠能与空气中的二氧化碳反应而变质,即二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,反应的化学方程式为CO2+2NaOH═Na2CO3+H2O.故答案为:CO2+2NaOH═Na2CO3+H2O;
【交流讨论】若氢氧化钠变质,生成的碳酸钠显碱性,也能使无色的酚酞试液变红色;故填:不能滴加酚酞试液,氢氧化钠溶液和碳酸钠溶液均显碱性,能使酚酞试液变红色;
【提出猜想】如果氢氧化钠完全反应掉,则溶质为碳酸钠;若部分参与反应,则溶质为碳酸钠和氢氧化钠;故填:碳酸钠;碳酸钠和氢氧化钠;
【实验验证】溶液中加入足量氯化钙溶液后,其中的碳酸钠与氯化钙反应产生了碳酸钙沉淀和氯化钠,过滤后再滴加酚酞,若存在氢氧化钠,溶液会变成红色;若没有氢氧化钠,则滴入酚酞试液后不变红.
故填:
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量大试管中的溶液于试管,加入足量CaCl2溶液,过滤 ②向滤液滴加适量无色酚酞试液 | 产生白色沉淀,溶液呈无色 | 猜想一正确 |
| 产生白色沉淀,溶液呈红色 | 猜想二正确 |
点评 此题在以往对中和反应探究考查的基础上又有所拓展,从定量研究的角度对同学们提出了要求.很多同学由于基础知识掌握不牢固,心理素质较差,缺乏分析推理和实验探究能力而不能顺利解答此类综合性问题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.规范的操作是实验成功的前提,下列实验操作正确的是( )
| A. | 取少量液体试剂时,滴管伸入试剂瓶内液体中,挤压胶头吸液 | |
| B. | 选用量程为50mL的量筒量取8mL液体 | |
| C. | 实验结束后,剩余的药品都必须放回原试剂瓶 | |
| D. | 洗净后的试管,放置晾干的正确方法是管口向下,并倒扣在试管架上 |
3.“分类”是科学学习和研究的重要方法之一,下列分类中不正确的是( )
| A. | 硫酸铜、食盐、纯碱属于盐 | B. | 硫酸铵、硝酸钾、尿素属于氮肥 | ||
| C. | 蛋白质、糖类、脂肪属于营养素 | D. | 杠杆、滑轮、斜面属于简单机械 |
10.下列各组物质中,俗名、化学名称和化学式所表示的是同一种物质的是( )
| A. | 纯碱 氢氧化钠 NaOH | B. | 水银 汞 Ag | ||
| C. | 胆矾 硫酸铜 CuSO4•5H2O | D. | 熟石灰 氢氧化钙 Ca(OH)2 |
7.下列现象中主要发生的是化学变化的是( )
| A. | 早读时,开灯室内变亮 | B. | 就餐时,咀嚼米饭变甜 | ||
| C. | 体育课上,把篮球投进筐中 | D. | 美术课上,捏个雕塑泥娃娃 |
2. 从哈市交警部门获悉,为了配合哈站改造项目配套建设一期工程的施工需要,我市将实施有史以来范围最大、时间跨度最长的一次交通流量大调整.下列有关叙述不正确的是( )
从哈市交警部门获悉,为了配合哈站改造项目配套建设一期工程的施工需要,我市将实施有史以来范围最大、时间跨度最长的一次交通流量大调整.下列有关叙述不正确的是( )
 从哈市交警部门获悉,为了配合哈站改造项目配套建设一期工程的施工需要,我市将实施有史以来范围最大、时间跨度最长的一次交通流量大调整.下列有关叙述不正确的是( )
从哈市交警部门获悉,为了配合哈站改造项目配套建设一期工程的施工需要,我市将实施有史以来范围最大、时间跨度最长的一次交通流量大调整.下列有关叙述不正确的是( )| A. | 部分路桥实施单双号通行政策,有利于缓解交通压力 | |
| B. | 在修建路桥的过程中,用到了许多钢筋、水泥、沙子,它们均属于金属材料 | |
| C. | 在路桥建设中,使用了生铁和钢,其中生铁的含碳量比钢高 | |
| D. | 道路建设中使用了许多沥青,是石油炼制的产品 |
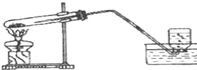 如图是实验室用高锰酸钾制取氧气的实验器装置,写出该反应的文字表达式.如图中有三个主要错误,它们是:
如图是实验室用高锰酸钾制取氧气的实验器装置,写出该反应的文字表达式.如图中有三个主要错误,它们是: