题目内容
14.资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物,某同学设计了如下实验方案,验证反应产物并探究发生反应的化学方程式.已知:①MgCO3和Mg(OH)2均为白色不溶物.
②MgCO3和Mg(OH)2均可跟盐酸发生复分解反应.
③酚酞遇碳酸氢钠溶液呈浅红色,酚酞遇碳酸钠溶液呈红色.
④CaCl2+Na2CO3═CaCO3↓+2NaCl
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能是MgCO3.
猜测2:白色不溶物可能是Mg(OH)2.
猜测3:白色不溶物可能是MgCO3和Mg(OH)2.
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体为氢气 |
| 实验Ⅲ | ①取实验Ⅰ中少量的白色悬浊液,过滤,洗涤干净沉淀,然后稀盐酸 | ②产生气泡,沉淀全部溶解 | 白色不溶物含有MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 有白色沉淀产生 | ③澄清液中一定含有的溶质是Na2CO3(化学式) |
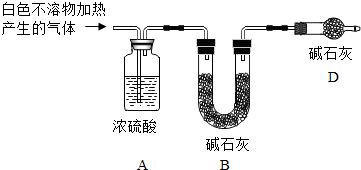
已知:MgCO3$\frac{\underline{\;\;△\;\;}}{\;}$MgO+CO2↑ Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O 碱石灰可以吸收二氧化碳和水蒸气
①如图所示实验装置D中碱石灰的作用是防止空气中的二氧化碳和水蒸气被B中碱石灰吸收,造成实验误差.
②称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中.实验前后装置A增重1.8g,装置B增重8.8g,可以证明猜想成立猜测3.
分析 (1)根据猜想可知,白色不溶物可能是氢氧化镁,可能是碳酸镁,也可能是碳酸镁和氢氧化镁的混合物进行分析;
(2)根据碳酸镁不溶于水,溶于酸,会与酸反应生成二氧化碳气体,氯化钙和碳酸钠反应会生成白色的碳酸钙沉淀进行分析;
(3)①根据B中碱石灰质量的增加量就是生成的二氧化碳的质量,取用B不能直接与空气接触,为了防止空气中的水蒸气和二氧化碳进入装置B中,影响实验结果,在B装置的尾部连接一个吸收空气中二氧化碳和水蒸气的装置进行分析;
②根据B中碱石灰增加的质量就是生成的二氧化碳,然后计算出碳酸镁的质量,剩余的固体就是氢氧化镁的质量,然后结合前面的验证书写化学方程式.
解答 解:(1)依据猜想可知,白色不溶于可能是氢氧化镁,可能是碳酸镁,也可能是碳酸镁和氢氧化镁的混合物,化学式为:MgCO3和Mg(OH)2的混合物;
(2)碳酸镁不溶于水,溶于酸,会与酸反应生成二氧化碳气体,氯化钙和碳酸钠反应会生成白色的碳酸钙沉淀,所以:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体为氢气 |
| 实验Ⅲ | ①取实验Ⅰ中少量的白色悬浊液,过滤,洗涤干净沉淀,然后 稀盐酸 | ②产生气泡,沉淀全部溶解 | 白色不溶物含有MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 有白色沉淀产生 | ③澄清液中一定含有的溶质是 Na2CO3(化学式) |
②B中碱石灰增加的质量就是生成的二氧化碳,所以生成的二氧化碳质量就是8.8g,
设生成8.8g二氧化碳,需要碳酸镁的质量为x,
MgCO3+2HCl=MgCl2+H2O+CO2↑
84 44
x 8.8g
则$\frac{84}{44}=\frac{x}{8.8g}$,解得x=16.8g.
所以生成氢氧化镁的质量为:22.6g-16.8g=5.8g;
则白色不溶物组成是MgCO3和Mg(OH)2,故可以证明猜想3成立.
故答案为:
(1)MgCO3和Mg(OH)2的混合物;(2)
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | |||
| 实验Ⅲ | 稀盐酸 | 产生气泡,沉淀全部溶解 | |
| 实验Ⅳ | Na2CO3 |
点评 本题难度较大,考查全面,从定性和定量两个方面确定物质的种类,关键在于知道碳酸根离子与酸反应能产生二氧化碳,镁和氢离子反应会生成氢气等知识进行分析.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
5.下列各组离子在水中能大量共存的是( )
| A. | Na+、H+、Cl-、HCO3- | B. | NH4+、Cu2+、NO3-、Cl- | ||
| C. | H+、Na+、OH-、SO42- | D. | Ag+、Ca2+、Cl-、NO3- |
9.通过实验可以获取证据,得出结论.下列做法中不能获得明显证据的是( )
| A. | 为了证明物质中含碳酸盐,在其溶液中滴加稀盐酸,然后将气体通入澄清石灰水 | |
| B. | 为了证明二氧化碳是否集满,把燃着的木条伸到集气瓶口 | |
| C. | 为了说明盐溶液不一定都呈中性,在氯化钠溶液中滴加酚酞试液 | |
| D. | 为了证明某瓶气体是否是二氧化硫,向集气瓶中倒入少量高锰酸钾溶液并摇晃 |
19.某化学兴趣小组做完“木炭还原氧化铜”的实验后,取4.0g混合物放入烧杯中,加入一定质量溶质质量分数为7.3%的稀盐酸,恰好得到蓝色滤液.有关数据如下表:
(1)过滤所得滤渣中一定含有铜.
(2)计算固体混合物中氧化铜的质量.
| 反应前物质的质量/g | 反应后物质的质量/g | |
| 固体混合物 | 稀盐酸 | 蓝色滤液 |
| 4.0 | 未知质量 | 10.8 |
(2)计算固体混合物中氧化铜的质量.
6.下列物质的用途主要与它的物理性质有关的是( )
| A. | 氧气用于炼钢 | B. | 干冰用于人工降雨 | ||
| C. | 氮气用作保护气 | D. | 稀盐酸用于除铁锈 |
3. 现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由弱到强的顺序是( )
现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由弱到强的顺序是( )
 现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由弱到强的顺序是( )
现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由弱到强的顺序是( )| A. | 甲 丙 乙 | B. | 丙 甲 乙 | C. | 乙 甲 丙 | D. | 甲 乙 丙 |

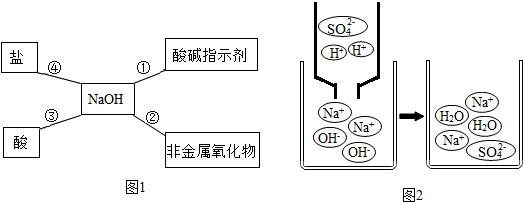
 某同学利用如图装置完成以下实验(加热装置已略去).
某同学利用如图装置完成以下实验(加热装置已略去).