题目内容
2.归纳总结是学习化学的重要方法,小明同学用图1总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).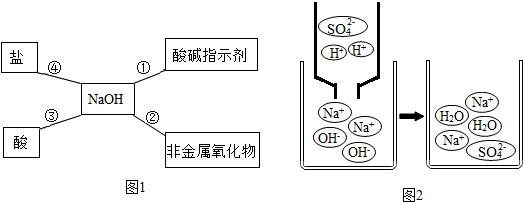
①验证反应①:小明将无色酚酞溶液滴入NaOH溶液中,溶液变成红色.
②小明用微观示意图2来说明反应③的发生,用化学反应方程式表示为2NaOH+H2SO4=Na2SO4+2H2O,从该图中可以看出,反应后的溶液pH=7(填“>”、“<”或“=”).
③请你写出一个化学反应方程式,满足反应④能够发生2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,该反应属于复分解反应.
分析 ①根据酸碱指示剂遇到酸碱的变色进行分析;
②根据围观图示中的微粒图示进行分析;
③根据盐的定义和复分解反应的含义进行分析.
解答 解:①碱会使酚酞变红色.故答案为:红色;
②容器中是氢氧根离子和钠离子,加入的是硫酸根离子和氢离子,所以反应物是氢氧化钠和硫酸,生成物中有钠离子、硫酸根离子和水分子,所以生成物是硫酸钠和水,故化学反应方程式表示为:2NaOH+H2SO4=Na2SO4+2H2O;根据反应后的容器中有钠离子、硫酸根离子和水分子,所以溶液显中性,溶液的pH值等于7,故答案为:2NaOH+H2SO4=Na2SO4+2H2O;=;
③反应④是盐和氢氧化钠反应,硫酸铜属于盐,且能和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式为为:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,是两种化合物相互交换成分生成另外的两种化合物,属于复分解反应.故填:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;复分解.
点评 在解此类题时,首先分析图示所表示的反应的实质,然后结合学过的知识和复分解反应的条件进行解答.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
10.在以下四种金属中,有一种金属的盐溶液与其它三种金属都能发生置换反应,这种金属是( )
| A. | Al | B. | Cu | C. | Fe | D. | Ag |
7.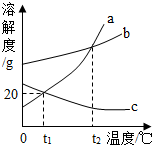 如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )
 如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )| A. | t1℃时,50g水中最多能溶解10ga | |
| B. | 将t1℃时的c的饱和溶液升温,变为不饱和溶液 | |
| C. | a中含有少量b时,可以用降温结晶法提纯a | |
| D. | a、c的饱和溶液从t2℃降温到t1℃时,两种溶液的溶质质量分数:a>c |
14.资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物,某同学设计了如下实验方案,验证反应产物并探究发生反应的化学方程式.
已知:①MgCO3和Mg(OH)2均为白色不溶物.
②MgCO3和Mg(OH)2均可跟盐酸发生复分解反应.
③酚酞遇碳酸氢钠溶液呈浅红色,酚酞遇碳酸钠溶液呈红色.
④CaCl2+Na2CO3═CaCO3↓+2NaCl
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能是MgCO3.
猜测2:白色不溶物可能是Mg(OH)2.
猜测3:白色不溶物可能是MgCO3和Mg(OH)2.
(2)设计定性实验确定产物并验证猜测:
(3)为进一步确定实验I的产物,设计定量实验方案,如图所示:
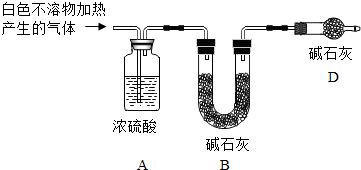
已知:MgCO3$\frac{\underline{\;\;△\;\;}}{\;}$MgO+CO2↑ Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O 碱石灰可以吸收二氧化碳和水蒸气
①如图所示实验装置D中碱石灰的作用是防止空气中的二氧化碳和水蒸气被B中碱石灰吸收,造成实验误差.
②称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中.实验前后装置A增重1.8g,装置B增重8.8g,可以证明猜想成立猜测3.
已知:①MgCO3和Mg(OH)2均为白色不溶物.
②MgCO3和Mg(OH)2均可跟盐酸发生复分解反应.
③酚酞遇碳酸氢钠溶液呈浅红色,酚酞遇碳酸钠溶液呈红色.
④CaCl2+Na2CO3═CaCO3↓+2NaCl
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能是MgCO3.
猜测2:白色不溶物可能是Mg(OH)2.
猜测3:白色不溶物可能是MgCO3和Mg(OH)2.
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体为氢气 |
| 实验Ⅲ | ①取实验Ⅰ中少量的白色悬浊液,过滤,洗涤干净沉淀,然后稀盐酸 | ②产生气泡,沉淀全部溶解 | 白色不溶物含有MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 有白色沉淀产生 | ③澄清液中一定含有的溶质是Na2CO3(化学式) |

已知:MgCO3$\frac{\underline{\;\;△\;\;}}{\;}$MgO+CO2↑ Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O 碱石灰可以吸收二氧化碳和水蒸气
①如图所示实验装置D中碱石灰的作用是防止空气中的二氧化碳和水蒸气被B中碱石灰吸收,造成实验误差.
②称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中.实验前后装置A增重1.8g,装置B增重8.8g,可以证明猜想成立猜测3.
12.下列食物富含糖类的是( )
| A. | 米饭 | B. | 黄瓜 | C. | 牛肉 | D. | 植物油 |

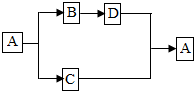 A~D都是初中化学中的常见物质,且有如图所示的转化关系(反应条件、部分反应物和生成物均已略去),请按照要求回答:
A~D都是初中化学中的常见物质,且有如图所示的转化关系(反应条件、部分反应物和生成物均已略去),请按照要求回答: