题目内容
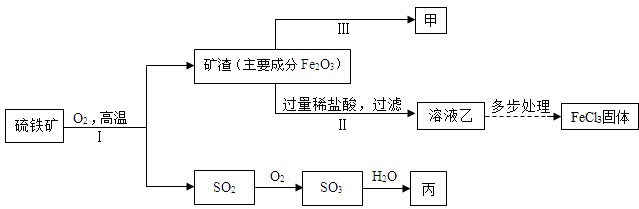
9.钢铁工业是一个国家的支柱产业之一.如图1是工业炼铁的基本生产流程示意图.某同学采集了一些生铁样品(含杂质,杂质不溶于水,不与稀硫酸反应)采用如图2所示装置进行分析.分别称得锥形瓶与棉花的质量为44.1g,生铁样品的质量为9.0g.在锥形瓶中加入适量稀硫酸后,立即开始记录电子天平的示数,记录数据如图3.请认真分析数据,回答下列问题: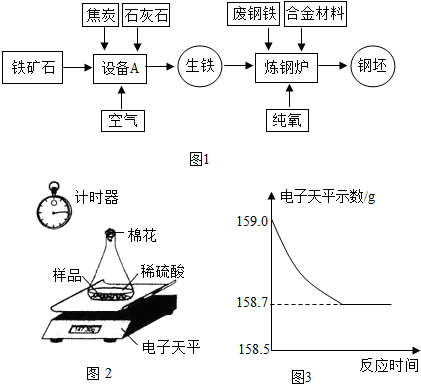
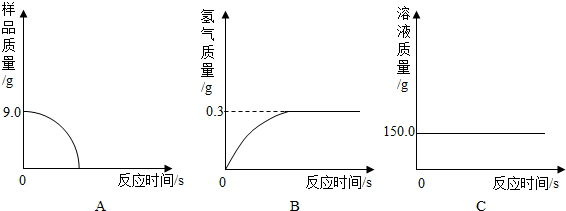
(1)小军数据处理的图象中正确的是B.
(2)计算样品中铁的质量(请写明过程).
(3)若所加的稀硫酸与铁恰好完全反应,计算硫酸溶液的溶质质量分数(请写明过程).
分析 根据反应记录数据,完全反应放出氢气质量=159.0g-158.7g=0.3g,加入稀硫酸的质量=159.0g-44.1g-9.0g=105.9g;结合反应的化学方程式,由生成氢气的质量计算生铁中铁的质量、反应生成硫酸亚铁的质量等,完成分析和计算.
解答 解:(1)由于生铁样品中的杂质不溶于水且不与酸发生反应,因此反应停止后样品的质量不为0;所以图A所示的分析错误;
随着生铁不断与稀硫酸反应,放出氢气质量逐渐增大,至完全反应,放出氢气的质量=159.0g-158.7g=0.3g;所以图B的分析正确;
加入稀硫酸的质量=159.0g-44.1g-9.0g=105.9g,反应使溶液的质量逐渐增大,直到反应停止溶液质量不再改变;所以图C的分析错误;
故选:B;
(2)(2)解:设反应的铁的质量为x
Fe+H2SO4═FeSO4+H2↑
56 2
x 0.3g
得出x=8.4g
(3)设硫酸溶液中溶质硫酸的质量为y
Fe+H2SO4═FeSO4+H2↑
98 2
y 0.3g
得出 y=14.7g
硫酸溶液的质量为159g-44.1g-9g=105.9g
硫酸溶液的溶质质量分数为14.7g/105.9g×100%=13.9%.
故答案为:(1)B;
(2)样品中铁的质量8.4g;
(3)硫酸溶液的溶质质量分数13.9%.
点评 根据质量守恒定律,反应后所得溶液的质量=所加稀盐酸的质量+参加反应铁的质量-放出氢气的质量.

练习册系列答案
相关题目
13.在CuCl2和ZnCl2的混合液中加过量的铁粉,充分反应后过滤,留在滤纸上的物质是( )
| A. | Cu | B. | Fe | C. | Cu和Zn | D. | Cu和Fe |
14.为测定绿矾FeSO4•xH2O中的x的值,某同学将一定量的绿矾放入坩埚内灼烧脱水.,生成无水FeSO4,测得有关数据为:
请写出计算x的数学表达式$\frac{{W}_{2}-W}{{W}_{1}{-}_{{W}_{2}}}$═$\frac{1×152}{18x}$.
| 质量/g | |
| 坩埚 | W |
| 坩埚+FeSO4•xH2O | W1 |
| 坩埚+FeSO4 | W2 |
4. 为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )
为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )
 为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )
为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )| A. | 依次通入无水硫酸铜,澄清石灰水,浓硫酸,甲装置,无水硫酸铜,澄清石灰水 | |
| B. | 依次通入无水硫酸铜,澄清石灰水,甲装置,无水硫酸铜,澄清石灰水 | |
| C. | 依次通入澄清石灰水,无水硫酸铜,浓硫酸,甲装置,无水硫酸铜,澄清石灰水 | |
| D. | 依次通入无水硫酸铜,澄清石灰水,浓硫酸,甲装置,澄清石灰水,无水硫酸铜 |
14.配制溶质质量分数为5%的下列溶液,能达到目的是( )
| A. | 称取5.0g氯化钾,溶解在95mL水中,充分搅拌 | |
| B. | 量取5.0mL过氧化氢溶液,放入入95mL水中,充分搅拌 | |
| C. | 量取5.0mL浓盐酸,倒入95mL水中,充分搅拌 | |
| D. | 称取5.0g碳酸钙,放入95mL水中,充分搅拌 |
1.如图为四种粒子的结构示意图,以下对相关粒子的描述不正确的是( )
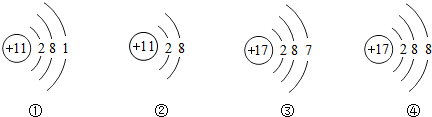
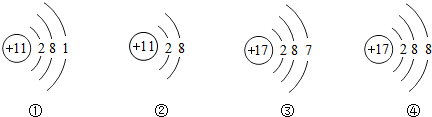
| A. | ①②属于同种元素 | B. | ②④具有相对稳定结构 | ||
| C. | ①③都容易失去电子 | D. | ②④形成的化合物为NaCl |
19.我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低.相关的下列说法中,正确的是( )
| A. | 不同浓度的亚硝酸盐会使萘胺显不同颜色 | |
| B. | 二氧化钛中Ti的化合价为+2 | |
| C. | 萘胺的相对分子质量为143克 | |
| D. | 这种试纸是一种新型化合物 |