题目内容
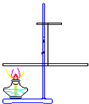 某兴趣小组为了探究质量守恒定律,进行了如图所示的小实验.在一根吊着的长玻璃棒两端,分别绕上铜丝(如图),并使该玻璃棒保持平衡.然后,用酒精灯给一端铜丝加热1-2分钟.停止加热后冷却,请回答下列问题:
某兴趣小组为了探究质量守恒定律,进行了如图所示的小实验.在一根吊着的长玻璃棒两端,分别绕上铜丝(如图),并使该玻璃棒保持平衡.然后,用酒精灯给一端铜丝加热1-2分钟.停止加热后冷却,请回答下列问题:(1)铜丝在空气中加热反应生成氧化铜,反应的化学方程式为
(2)请画图并说明此时玻璃棒是否平衡(酒精灯和铁架台不用画)
图:
说明:
考点:质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:用酒精灯给左边一端铜丝加热,铜会与空气中氧气发生反应,根据反应物与生成物的比较得出实验现象,由于铜与氧气发生反应生成了氧化铜,所以左端质量大了.
解答:解:
(1)反应物为铜和氧气,生成物为氧化铜,反应条件是加热,用观察法配平即可.其化学方程式为:2Cu+O2
2CuO.
(2)图:玻璃棒左端(或被加热端)下沉.或被玻璃棒右端(或未加热端)上升.
说明:铜丝原来的质量只是铜的质量,加热后变成了氧化铜,故左端的质量增加了,向左倾斜;
故答案为:
(1)2Cu+O2
2CuO;
(2)①如图;②铜丝原来的质量只是铜的质量,加热后变成了氧化铜,故左端的质量增加了,向左倾斜
(1)反应物为铜和氧气,生成物为氧化铜,反应条件是加热,用观察法配平即可.其化学方程式为:2Cu+O2
| ||
(2)图:玻璃棒左端(或被加热端)下沉.或被玻璃棒右端(或未加热端)上升.

说明:铜丝原来的质量只是铜的质量,加热后变成了氧化铜,故左端的质量增加了,向左倾斜;
故答案为:
(1)2Cu+O2
| ||
(2)①如图;②铜丝原来的质量只是铜的质量,加热后变成了氧化铜,故左端的质量增加了,向左倾斜
点评:通过回答本题可知如果有质量增加的化学反应,也符合质量守恒定律,只要是质量增加了,肯定有别的物质参加了反应;书写方程式时要熟记书写步骤:一写二配三注明四等号.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
有新物质生成的变化是( )
| A、海水晒盐 | B、牛奶制酸奶 |
| C、液态空气制氧 | D、干冰气化 |


 请你回答在实验室用高锰酸钾制取氧气(用排水法收集)的下列问题.
请你回答在实验室用高锰酸钾制取氧气(用排水法收集)的下列问题.