题目内容
硝酸铵的化学式为NH4NO3,试计算:
(1)硝酸铵的相对分子质量为 .
(2)硝酸铵中:氮、氧二种元素的质量比为 .
(3)其中氮元素的质量分数为 (写出计算过程).
(4)40Kg硝酸铵中含氮 Kg.
(1)硝酸铵的相对分子质量为
(2)硝酸铵中:氮、氧二种元素的质量比为
(3)其中氮元素的质量分数为
(4)40Kg硝酸铵中含氮
考点:相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=
×100%,进行分析解答.
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:
(1)硝酸铵的相对分子质量为14×2+1×4+16×3=80.
(2)硝酸铵中氮、氧元素的质量比为(14×2):(16×3)=7:12.
(3)其中氮元素的质量分数为
×100%=35%.
(4)40kg硝酸铵中含氮元素的质量为40kg×35%=14kg.
故答案为:(1)80;(2)7:12;(3)35%;(4)14.
(1)硝酸铵的相对分子质量为14×2+1×4+16×3=80.
(2)硝酸铵中氮、氧元素的质量比为(14×2):(16×3)=7:12.
(3)其中氮元素的质量分数为
| 14×2 |
| 80 |
(4)40kg硝酸铵中含氮元素的质量为40kg×35%=14kg.
故答案为:(1)80;(2)7:12;(3)35%;(4)14.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
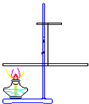 某兴趣小组为了探究质量守恒定律,进行了如图所示的小实验.在一根吊着的长玻璃棒两端,分别绕上铜丝(如图),并使该玻璃棒保持平衡.然后,用酒精灯给一端铜丝加热1-2分钟.停止加热后冷却,请回答下列问题:
某兴趣小组为了探究质量守恒定律,进行了如图所示的小实验.在一根吊着的长玻璃棒两端,分别绕上铜丝(如图),并使该玻璃棒保持平衡.然后,用酒精灯给一端铜丝加热1-2分钟.停止加热后冷却,请回答下列问题: