题目内容
14.在学习盐的性质时,同学对碳酸钠溶液与氢氧化钙溶液反应后,过滤得到的澄清滤液,提出了问题:过滤后澄清滤液中会有哪些溶质?为此他们进行了如下的探究活动,请你共同参与并回答相关问题.(1)写出所发生反应的化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(2)【提出猜想】猜想一:滤液中溶质是NaOH 和Na2CO3
猜想二:滤液中溶质是NaOH和Ca(OH)2
猜想三:滤液中溶质是NaOH
(3)【方案设计】设计实验方案确定滤液中溶质的组成.
(4)
方法一:
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入Ca(OH)2溶液,B中加入碳酸钠溶液,观察现象. | A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
若A中没有沉淀,B中产生白色沉淀 | “猜想二”成立 | |
若A、B两支试管中都没有沉淀产生 | “猜想三”成立 |
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,滴入足量稀盐酸 | 有气泡产生 | “猜想一”成立 |
分析 (1)氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠;
(2)根据反应的过程以及反应物是否过量来分析;
(4)根据检验氢氧化钙存在用碳酸钠,检验碳酸钠存在用氢氧化钙来分析;
若猜想一成立,加入过量的稀盐酸后,先与氢氧化钠反应,然后再与碳酸钠反应.
解答 解:(1)氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠;
故填:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(2)可能二者恰好完全反应,也可能氢氧化钙或碳酸钠有剩余,故填:猜想二:NaOH和Ca(OH)2
(4)检验氢氧化钙是否存在可以加入碳酸钠溶液观察是否产生白色沉淀;检验碳酸钠存在可以加入氢氧化钙溶液,观察是否产生白色沉淀;故答案为:
方法一
| 实验操作 | 实验现象 |
| Na2CO3 | 若A中没有沉淀,B中产生白色沉淀 |
| 若A、B两支试管中都没有沉淀产生 |
故填:方法二:有气泡产生
点评 本题为典型的实验探究中的实验分析题,只有熟练掌握所学知识才能明白实验的设计,才能顺利得出正确答案.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17. 今年五月,泰安对餐饮食品抽检,45%的大米被检出重金属镉超标.如图A为周期表中的镉元素,图B为镉原子结构示意图,下列说法正确的是( )
今年五月,泰安对餐饮食品抽检,45%的大米被检出重金属镉超标.如图A为周期表中的镉元素,图B为镉原子结构示意图,下列说法正确的是( )
 今年五月,泰安对餐饮食品抽检,45%的大米被检出重金属镉超标.如图A为周期表中的镉元素,图B为镉原子结构示意图,下列说法正确的是( )
今年五月,泰安对餐饮食品抽检,45%的大米被检出重金属镉超标.如图A为周期表中的镉元素,图B为镉原子结构示意图,下列说法正确的是( )| A. | 镉原子的相对原子质量为112.4g | |
| B. | 符号“Cd”可以表示金属镉、一个镉原子 | |
| C. | 金属镉能使蛋白质失去生理活性 | |
| D. | 镉位于周期表的第五周期,图B中X=4 |
5.某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:
①CuSO4溶液与NaOH溶液、②CuSO4溶液与BaCl2溶液反应.实验结束后将两次实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.
(1)取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液为紫色,则滤液呈中性(填“酸”、“中”、“碱”).
(2)废液在烧杯中混合后,肯定发生的化学反应的方程式:2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】小红认为:只含氯化钠; 小明认为:可能含有硫酸钠、氯化钠和氯化钡;
小亮认为:可能含氯化钠和氯化钡; 你认为:还可能是氯化钠和硫酸钠(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想明显不合理?为什么?小明,硫酸钠和氯化钡不能共存.
【实验探究】
①CuSO4溶液与NaOH溶液、②CuSO4溶液与BaCl2溶液反应.实验结束后将两次实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.
(1)取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液为紫色,则滤液呈中性(填“酸”、“中”、“碱”).
(2)废液在烧杯中混合后,肯定发生的化学反应的方程式:2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】小红认为:只含氯化钠; 小明认为:可能含有硫酸钠、氯化钠和氯化钡;
小亮认为:可能含氯化钠和氯化钡; 你认为:还可能是氯化钠和硫酸钠(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想明显不合理?为什么?小明,硫酸钠和氯化钡不能共存.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 实验A:取少量滤液于试管中,加入适量纯碱溶液,振荡. | 无明显现象 | 滤液中不含氯化钡 |
| 实验B:取少量滤液于试管中,加入适量硝酸钡溶液,振荡. | 产生白色沉淀 | 滤液中含有硫酸钠 |
2.下列操作中,不正确的是( )
| A. | 给试管里的液体加热时,试管口对着没有人的方向 | |
| B. | 用胶头滴管向试管中滴加液体时,把滴管伸入试管内 | |
| C. | 在实验室里制取氢气,先检查装置的气密性 | |
| D. | 浓硫酸沾到皮肤上,要立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液 |
19.如图是干燥、收集某气体的装置,由实验装置可以推测该气体的有关性质.请你在表中找出相对应的选项( )
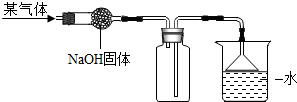

| 气体性质\序号 | A | B | C | D |
| 溶于水中所得溶液的pH | >7 | <7 | >7 | <7 |
| 其密度(ρ1)与空气密度(ρ2)比较 | ρ1>ρ2 | ρ1>ρ2 | ρ1<ρ2 | ρ2<ρ1 |
| 在水中的溶解度 | 极易溶 | 难溶 | 极易溶 | 难溶 |
| A. | A | B. | B | C. | C | D. | D |
17.水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水.)
有关实验数据如下表:
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为4.4g.
(2)求12g克该石灰石中碳酸钙的质量是多少克?
(3)该石灰石中碳酸钙的质量分数为83.3%(结果保留一位小数)
有关实验数据如下表:
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12g | 157.6g | |
(2)求12g克该石灰石中碳酸钙的质量是多少克?
(3)该石灰石中碳酸钙的质量分数为83.3%(结果保留一位小数)
18.奇妙的化学,几乎无处不在,时刻影响着我们的生活,不断推动着人类社会向前发展.下列 过程中没有发生化学变化的是( )
| A. | 生石灰制熟石灰 | B. | 热法淡化海水 | C. | 高粱制成烧酒 | D. | 铁矿石炼成铁 |