题目内容
19.如图是干燥、收集某气体的装置,由实验装置可以推测该气体的有关性质.请你在表中找出相对应的选项( )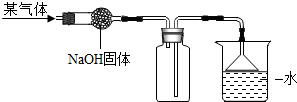
| 气体性质\序号 | A | B | C | D |
| 溶于水中所得溶液的pH | >7 | <7 | >7 | <7 |
| 其密度(ρ1)与空气密度(ρ2)比较 | ρ1>ρ2 | ρ1>ρ2 | ρ1<ρ2 | ρ2<ρ1 |
| 在水中的溶解度 | 极易溶 | 难溶 | 极易溶 | 难溶 |
| A. | A | B. | B | C. | C | D. | D |
分析 由收集装置可知,氢氧化钠固体可以干燥碱性气体,该气体的密度比空气小,从吸收装置分析可知,该气体易溶于水.
解答 解:由收集装置可知,氢氧化钠固体可以干燥碱性气体,溶于水中所得溶液的pH>7;当该气体的密度比空气小时,可以把集气瓶中的空气顺利排出;吸收装置中,导管连接了一个漏斗,目的是为了防止倒吸,说明该气体极易溶于水.
故选C.
点评 本题考查了分析实验的能力,从多角度对气体的收集方法进行了综合考查,考虑收集气体的方法时,应该从气体的密度、水溶性等角度进行分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列物质属于纯净物的是( )
| A. | 合金 | B. | 石灰水 | C. | 金刚石 | D. | 铁锈 |
10.下列实验操作中,正确的是( )
| A. |  倾倒液体 | B. | 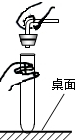 连接仪器 | C. |  稀释浓硫酸 | D. |  取用石灰石 |
7.下列实验方案能达到目的是( )
| A. | 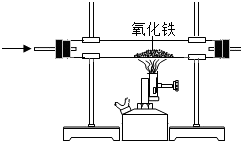 除去CO中的CO2 除去CO中的CO2 | B. | 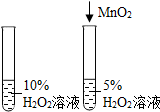 探究二氧化锰对反应速率的影响 探究二氧化锰对反应速率的影响 | ||
| C. | 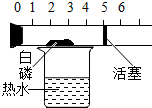 探究空气中氧气的含量 探究空气中氧气的含量 | D. | 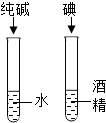 探究影响物质溶解性的因素 探究影响物质溶解性的因素 |
14.在学习盐的性质时,同学对碳酸钠溶液与氢氧化钙溶液反应后,过滤得到的澄清滤液,提出了问题:过滤后澄清滤液中会有哪些溶质?为此他们进行了如下的探究活动,请你共同参与并回答相关问题.
(1)写出所发生反应的化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(2)【提出猜想】猜想一:滤液中溶质是NaOH 和Na2CO3
猜想二:滤液中溶质是NaOH和Ca(OH)2
猜想三:滤液中溶质是NaOH
(3)【方案设计】设计实验方案确定滤液中溶质的组成.
(4)
方法一:
方法二:针对猜想一,另一同学提出了新的方案.
【实验验证】依据上述设计,通过实验验证,最终得出的结论是猜想一正确.
(1)写出所发生反应的化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(2)【提出猜想】猜想一:滤液中溶质是NaOH 和Na2CO3
猜想二:滤液中溶质是NaOH和Ca(OH)2
猜想三:滤液中溶质是NaOH
(3)【方案设计】设计实验方案确定滤液中溶质的组成.
(4)
方法一:
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入Ca(OH)2溶液,B中加入碳酸钠溶液,观察现象. | A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
若A中没有沉淀,B中产生白色沉淀 | “猜想二”成立 | |
若A、B两支试管中都没有沉淀产生 | “猜想三”成立 |
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,滴入足量稀盐酸 | 有气泡产生 | “猜想一”成立 |
4.除去下列物质中的少量杂质,所用试剂或方法不正确的是( )
| 选项 | 物质 | 杂质 | 试剂或方法 |
| A | CO | H2 | 通入O2中点燃 |
| B | N2 | O2 | 通过足量灼热的铜丝 |
| C | KNO3溶液 | Ba(NO3)2 | 滴加适量K2SO4溶液,过滤 |
| D | NaCl溶液 | Na2CO3 | 滴加稀盐酸至不再产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
2.下面对某些实验现象的描述,不正确的是( )
| A. | 鸡蛋壳能溶于醋酸,并产生气泡 | |
| B. | CuSO4溶液中滴入氨水,产生蓝色沉淀 | |
| C. | H2还原CuO,固体由黑色变为红色,并有水珠生成 | |
| D. | 铁丝在纯氧中燃烧,火星四射,产生红棕色固体 |
 图中,A代表地壳中含量第二位的金属,C为黑色粉末,E在常温下为液态且为相对分子质量最小的氧化物.常温下,相连环物质间能发生反应,请填空.
图中,A代表地壳中含量第二位的金属,C为黑色粉末,E在常温下为液态且为相对分子质量最小的氧化物.常温下,相连环物质间能发生反应,请填空.