题目内容
2.对比学习有利于发现事物的共性与个性.为探究酸的化学性质,同学们进行了如下实验:| 实验内容 | 实验现象 | 分析与结论 |
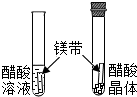 | 装有醋酸晶体试管内没有气泡冒出,装有醋酸溶液试管中镁带表面冒气泡. | 酸的很多反应通常在水溶液中才能完成. |
用玻璃棒蘸硫酸在白纸上写字 | 浓(填“浓”或“稀”)硫酸使白纸炭化. | 即使是同种酸,由于浓度不同,它们的性质不完全相同. |
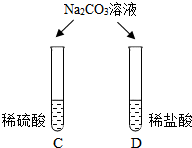 | 两试管中均产生气泡 | 不同的酸具有相似的性质,这是因为酸的溶液中都含有H+(填化学符号). |
 | E试管中产生白色沉淀, F试管中无明显现象. | 不同的酸根会导致酸的“个性”差异.因此,可用氯化钡溶液鉴别盐酸和硫酸. |
Ⅰ.废液缸中产生气体的化学方程式为2HCl+Na2CO3═2NaCl+H2O+CO2↑.
Ⅱ.废液缸里最终产生的白色沉淀一定有BaSO4(填化学式).
分析 根据题干提供的实验现象结合已有的物质的性质进行分析解答即可.
解答 解:醋酸晶体不与镁条反应,故没有气泡产生;浓硫酸能使白纸炭化,稀硫酸不能使白纸炭化,说明浓度不同,物质的性质不同;稀盐酸和稀硫酸都能与碳酸钠溶液反应产生气体,故都会观察到气泡产生,是因为稀盐酸和稀硫酸中都含有氢离子;稀硫酸能与氯化钡溶液反应产生硫酸钡白色沉淀;故填:
| 实验内容 | 实验现象 | 分析与结论 |
| 没有气泡冒出 | ||
| 浓 | 浓度 | |
| 气泡 | H+ | |
| 白色沉淀 |
Ⅱ.废液缸里最终产生的白色沉淀一定有硫酸钡,因为硫酸钡是不溶于酸的沉淀,故填:BaSO4.
点评 本题为常见的酸的性质的实验探究,完成此题,可以依据已有的知识结合题干提供的信息进行.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
13.下列物质的性质与所对应的用途没有直接关系的是( )
| A. | 干冰升华吸热-----用于人工降雨 | |
| B. | 稀有气体的性质稳定------作保护气 | |
| C. | 石墨很软------用作电极 | |
| D. | 氢氧化钙呈碱性----用于改良酸性土壤 |
10.下列关于硝酸铵(NH4NO3)的说法,不正确的是( )
| A. | NH4NO3是一种常见的氮肥 | |
| B. | NH4NO3中含2种不同的原子团 | |
| C. | NH4NO3中各元素的质量比为1:4:1:3 | |
| D. | NH4NO3中氮元素的质量分数为$\frac{14×2}{14×2+1×4+16×3}$×100% |
11.下表列出了除去物质中所含少量杂质的方法,其中错误的是( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO2 | O2 | 通过灼热的铜网 |
| B | KOH溶液 | K2CO3 | 加入足量稀盐酸至不再产生气泡 |
| C | NaCl | CaCO3 | 溶解、过滤、蒸发 |
| D | H2 | HCl | 依次通过NaOH溶液和浓H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
 10.3gNaCl、Na2CO3的样品,放入烧杯中,加入50g水,充分溶解,再向烧杯中滴加氯化钙溶液,恰好反应完全.实验测得加入的氯化钙溶液和烧杯中物质溶液的质量关系如图所示.求:
10.3gNaCl、Na2CO3的样品,放入烧杯中,加入50g水,充分溶解,再向烧杯中滴加氯化钙溶液,恰好反应完全.实验测得加入的氯化钙溶液和烧杯中物质溶液的质量关系如图所示.求:




