题目内容
2. 某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热.
Ⅱ.将xgKClO3与1.0g CuO均匀混合加热.
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;Ⅱ中x的值应为3.0g.
(2)乙探究了影响双氧水分解速度的某种因素.反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,有关实验数据记录如下:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2质量 | |
| Ⅰ | 50.0g | 1% | 0.1g | 0.013mg |
| Ⅱ | 50.0g | 2% | 0.1g | 0.023mg |
| Ⅲ | 50.0g | 4% | 0.1g | 0.044mg |
实验结论:在相同条件下,反应物的浓度越大,双氧水分解得越快.
分析 根据已有的知识进行分析解答,氯酸钾在二氧化锰催化剂的作用下加热生成氯化钾和氧气,进行实验时要注意控制变量,保证氯酸钾的质量相同;过氧化氢在二氧化锰的催化作用下反应生成水和氧气,根据质量差计算生成氧气的质量,根据实验确定在条件相同的条件下,反应物的浓度越大,双氧水的分解越快,据此解答.
解答 解:(1)氯酸钾在二氧化锰催化剂的作用下加热生成氯化钾和氧气,进行实验时要注意控制变量,保证氯酸钾的质量相同,故x是3.0,故填:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,3.0g;
(2)过氧化氢在二氧化锰的催化作用下反应生成水和氧气,锥形瓶与反应物减少的质量即生成氧气的质量,根据实验确定在条件相同的条件下,反应物的浓度越大,双氧水的分解越快,故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,锥形瓶与反应物减少的质量即生成氧气的质量,反应物的浓度越大.
点评 本题考查的是化学反应速率的影响因素的实验探究,完成此题,可以依据题干提供的信息结合已有的知识进行.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
17.下列现象中,能说明某溶液呈碱性的是( )
| A. | 用pH试纸测定,其pH=6 | B. | 用pH试纸测定,其pH=7 | ||
| C. | 向其中滴加紫色石蕊溶液,呈红色 | D. | 向其中滴加无色酚酞溶液,呈红色 |
7.下列变化中属于化学变化的是( )
| A. | 水变成冰 | B. | 碘的升华 | C. | 氧气液化 | D. | 食物变质 |
11.下列物质分类正确的是( )
| A. | 水、空气、煤都是混合物 | B. | 石墨、盐水、铅、人体是导体 | ||
| C. | 沥青、食盐、铁、冰都是晶体 | D. | 硝酸钾、氯化钾、磷酸钾都是钾肥 |
12.下列知识整理的内容有错误的是( )
| A、实验方法 | B、化学与生活 |
| ①鉴别O2、CO2--可用澄清石灰水 ②熄灭酒精灯--用灯帽盖灭 ③除去水瓶中的水垢--用稀盐酸 | ①人体缺铁会引起贫血症 ②进入久未开启的菜窖时先做灯火实验 ③用活性炭净水器可净化水 |
| C、实验记录 | D、物质构成 |
| ①用10mL量筒量取8mL水 ②滴有紫色石蕊试液的水中通入CO2后 变红 ③用托盘天平称取5.6g食盐 | ①分子、原子、离子都是构成物质的微粒 ②空气、液氧、二氧化硫中都含有氧分子 ③碳酸钠的化学式为 NaCO3 |
| A. | A | B. | B | C. | C | D. | D |


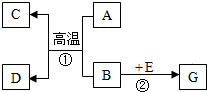 A~H是初中化学常见的物质,它们之间的相互关系如图所示,其中A是黑色粉末、B是红棕色粉末(一种铁矿石主要成分),C常温下为气体,G是一种盐.请回答下面问题:
A~H是初中化学常见的物质,它们之间的相互关系如图所示,其中A是黑色粉末、B是红棕色粉末(一种铁矿石主要成分),C常温下为气体,G是一种盐.请回答下面问题: