题目内容
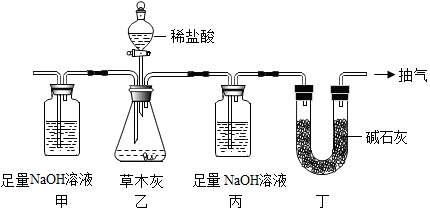
3.某校甲、乙两兴趣小组进行硫酸铜溶液与与氢氧化钠溶液的实验.甲组实验:先往试管中各加入2mL 10%的CuSO4溶液,再往试管中加入5mL 10%的NaOH溶液,观察到试管中有蓝色沉淀生成.
乙组实验:先往试管中各加入2mL 10%的CuSO4溶液,再往试管中加入2滴10%的NaOH溶液,观察到试管中有浅绿色沉淀生成(与甲组的沉淀颜色差别较大).
【实验讨论】甲组实验中的蓝色沉淀是氢氧化铜,写出反应的化学方程式:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4.
那么乙组实验中浅绿色沉淀是什么呢?
【查阅资料】
(1)NaOH溶液和CuSO4溶液反应可生成多种组成的碱式硫酸铜,它们都是浅绿色固体.如Cu2(OH)2SO4、Cu3(OH)4SO4或Cu4(OH)6SO4,它们的相对分子质量分别为258、356、454.
(2)各种组成的碱式硫酸铜,受热均会分解.
(3)SO2气体能使酸性高锰酸钾稀溶液褪色.
(4)白色的无水CuSO4固体吸收水蒸气后变成变蓝色固体.
【实验探究】该小组对碱式硫酸铜产生了兴趣,想探究碱式硫酸铜受热分解的产物.
【实验设计】取少量碱式硫酸铜加入试管中并按以下流程进行实验:
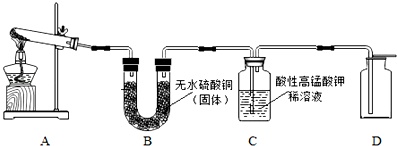
实验结束后,试管中残留有黑色固体,滴入稀硫酸黑色固体溶解,溶液呈蓝色,证明黑色固体是CuO;B中无水CuSO4变蓝色,证明有水(或H2O)生成;C中现象为酸性高锰酸钾溶液褪色,证明生成SO2;D中气体能使带火星木条复燃,证明生成O2.
【实验反思】
(1)当NaOH溶液和CuSO4溶液反应时,只要控制CuSO4溶液的量一定,NaOH溶液
不足(填“过量”或“不足”)时就能生成浅绿色沉淀.
(2)若碱式硫酸铜Cu3(OH)4SO4可表示为:2Cu(OH)2•CuSO4,则Cu4(OH)6SO4还可表示为:3Cu(OH)2•CuSO4.
【拓展延伸】
(1)当反应物相同,而反应物的量不同,产物可能不同.试另举一个例子:碳充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳.
(2)当反应物相同,而反应条件不同时,产物也可能不同.如常温下二氧化碳和水反应生成碳酸;在光照作用下,二氧化碳和水在植物的叶子中发生光合作用生成氧气.
(3)为了确定所得浅绿色沉淀的组成,再进行后续实验,取8.9g碱式硫酸铜(假设化学式为:aCu(OH)2•bCuSO4)放入试管中加热,充分反应后生成了0.9g水,通过计算确定所得浅绿色沉淀的化学式为Cu3(OH)4SO4.
分析 氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠;
根据实验现象可以判断物质的组成,根据物质的性质可以判断实验现象;
碳完全燃烧生成二氧化碳,不完全燃烧生成一氧化碳;
根据物质中氢元素的质量分数及其提供的数据可以判断物质的组成.
解答 解:【实验讨论】
得到的蓝色沉淀一定是氢氧化铜,氢氧化钠和硫酸铜反应的化学方程式为:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓.
故填:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓.
【实验设计】
B中无水CuSO4变蓝色,证明有有水生成;由于SO2气体能使酸性高锰酸钾稀溶液褪色,所以C中酸性高锰酸钾溶液褪色,证明生成SO2.
【实验反思】
(1)5mL氢氧化钠溶液的体积远远大于乙2滴氢氧化钠溶液的体积,因此NaOH溶液不足时就能生成浅绿色沉淀,此实验利用的科学方法是控制变量法.
(2)因为碱式硫酸铜可表示为aCu(OH)2•bCuSO4,则Cu4(OH)6SO4还可表示为:3Cu(OH)2•CuSO4.
故填:3Cu(OH)2•CuSO4.
【拓展延伸】
(1)当反应物的量不同,产物可能不同,例如碳燃烧时,氧气足量时生成二氧化碳,氧气不足时生成一氧化碳.
故填:碳燃烧时,氧气足量时生成二氧化碳,氧气不足时生成一氧化碳.
(2)根据常温下二氧化碳和水反应生成碳酸;在光照作用下,二氧化碳和水在植物的叶子中发生光合作用生成氧气,可知当反应物相同,而反应条件不同时,产物也可能不同.
故填:反应条件;
(3)0.9g水中氢元素的质量为:0.9g×$\frac{2}{18}×$100%═0.1g,
则碱式硫酸铜中氢元素的质量分数为:$\frac{0.1g}{8.9g}$×100%=1.12%,
Cu2(OH)2SO4中氢元素的质量分数为:$\frac{2}{258}$×100%=0.78%,
Cu3(OH)4SO4中氢元素的质量分数为:$\frac{4}{356}$×100%=1.12%,
Cu4(OH)6SO4中氢元素的质量分数为:$\frac{6}{454}$×100%=1.32%,
根据计算的结果可知,所得浅绿色沉淀的化学式为Cu3(OH)4SO4.
故填:Cu3(OH)4SO4.
答案:
CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
【实验设计】
水(或H2O); 酸性高锰酸钾稀溶液的紫色褪色(或紫色变浅)
【实验反思】
(1)不足;
(2)3Cu(OH)2•CuSO4
【拓展延伸】
(1)碳充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳(其他合理答案也可)
(2)反应条件;
(3)2Cu(OH)2•CuSO4 (或Cu3(OH)4SO4)
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | 部分元素原子序数关系: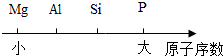 | |
| B. |  生活中常见物质的pH(常温下,中性溶液的pH为7,酸性溶液的pH<7,碱性溶液的pH>7): 生活中常见物质的pH(常温下,中性溶液的pH为7,酸性溶液的pH<7,碱性溶液的pH>7): | |
| C. | 地壳中部分元素的含量关系: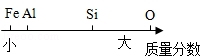 | |
| D. | 空气中部分成分的体积分数关系: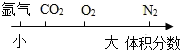 |
| A. | Cu | B. | Zn | C. | Fe | D. | A1 |
| A. | 过氧化钠(H2O2)和氧化钙(CaO)都属于氧化物 | |
| B. | 水和氢气都属于单质 | |
| C. | 碳酸钙(CaC03)和氢氧化钙(Ca(OH)2)都属于盐 | |
| D. | 火碱(NaOH)和碳酸钠(Na2CO3)都属于碱 |
| 选项 | 实验目的 | 实验操作 |
| A | 区别烧碱和食盐 | 取固体加水,并测定溶液的温度 |
| B | 检验氧气是否收集满 | 将带火星的木条放在集气瓶口,观察是否复燃 |
| C | 区别羊毛和化纤布料 | 取样品燃烧,闻气味 |
| D | 除去CO2中混有的HCl气体 | 将气体通过NaOH溶液后再通过浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
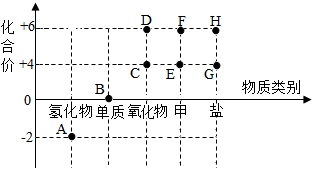 以物质类别为横坐标,以化合价为纵坐标,所绘制的图象叫价类图.如图为硫元素的价类图,根据图象回答:
以物质类别为横坐标,以化合价为纵坐标,所绘制的图象叫价类图.如图为硫元素的价类图,根据图象回答: 如表是元素周期表的一部分,氧原子的核外最外层电子数为6;等质量的氧气和氮气中,所含原子数较少的是氧气.
如表是元素周期表的一部分,氧原子的核外最外层电子数为6;等质量的氧气和氮气中,所含原子数较少的是氧气.