题目内容
6.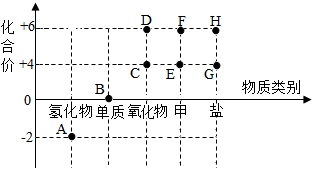 以物质类别为横坐标,以化合价为纵坐标,所绘制的图象叫价类图.如图为硫元素的价类图,根据图象回答:
以物质类别为横坐标,以化合价为纵坐标,所绘制的图象叫价类图.如图为硫元素的价类图,根据图象回答:(1)甲处表示的物质类别为酸
(2)C点表示的物质的化学式为SO2
(3)化合物FeSO4应处于价类图中的G点(填字母).
(4)F点所表示的物质与氯化钡溶液反应的化学方程式为BaCl2+H2SO4═BaSO4↓+2HCl.
分析 (1)由硫的价类图可知,甲处物质中硫元素的化合价为+4价、+6价,进行分析解答即可.
(2)C点表示的物质属于氧化物,且硫元素的化合价为+4价,进行分析解答.
(3)FeSO4是由亚铁离子和硫酸根离子构成的化合物,属于盐;铁元素显+2价,氧元素显-2价,硫元素显+4价;进行分析解答.
(4)F点所表示的物质是+6价铁的酸,应为硫酸,硫酸与氯化钡溶液反应生成硫酸钡沉淀和盐酸,写出反应的化学方程式即可.
解答 解:(1)由硫的价类图可知,甲处物质中硫元素的化合价为+4价、+6价,亚硫酸、硫酸中硫元素分别显+4价、+6价,甲处表示的物质类别为酸.
(2)C点表示的物质属于氧化物,且硫元素的化合价为+4价,氧元素显-2价,其化学式为:SO2.
(3)FeSO4是由亚铁离子和硫酸根离子构成的化合物,属于盐;铁元素显+2价,氧元素显-2价,硫元素显+4价,应处于价类图中的G点.
(4)F点所表示的物质是+6价铁的酸,应为硫酸,硫酸与氯化钡溶液反应生成硫酸钡沉淀和盐酸,反应的化学方程式为:BaCl2+H2SO4═BaSO4↓+2HCl.
故答案为:(1)酸;(2)SO2;(3)G;(4)BaCl2+H2SO4═BaSO4↓+2HCl.
点评 本题难度不大,理解价类图的含义、酸碱盐与单质、氧化物的特征等并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
14. 某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)
某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)
①操作I是过滤.
②在沉淀B中加入足量稀硝酸,沉淀部分溶解.根据上述实验分析,A中一定含有的物质是Na2CO3、Na2SO4、Ba(NO3)2.写出沉淀部分溶解的化学方程式BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑.
③取少量滤液C于试管中,滴入酚酞,溶液变红,则C中一定含有的溶质是NaNO3、Na2CO3.
④为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.
 某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)
某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)①操作I是过滤.
②在沉淀B中加入足量稀硝酸,沉淀部分溶解.根据上述实验分析,A中一定含有的物质是Na2CO3、Na2SO4、Ba(NO3)2.写出沉淀部分溶解的化学方程式BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑.
③取少量滤液C于试管中,滴入酚酞,溶液变红,则C中一定含有的溶质是NaNO3、Na2CO3.
④为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.
| 实验操作 | 现象 | 结论 |
| 取滤液C少量,滴入足量Ba(NO3)2溶液;过滤后往滤液中滴入AgNO3溶液 | 产生白色沉淀 | 确定A固体中还含有氯化钠 |
1.甲、乙分别是碳酸钠和氯化钠中的一种物质.如图1是两物质的溶解度曲线.如图2是20℃时,将等质量甲、乙两种固态分别放入盛有等质量水的两支试管中,甲没有完全溶解,乙全部溶解.
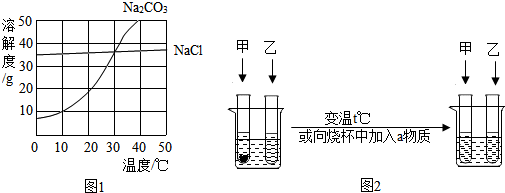
下列说法正确的是( )

下列说法正确的是( )
| A. | t℃>20℃ | |
| B. | a物质可能是NH4NO3 | |
| C. | 甲物质为NaCl | |
| D. | 10℃时,等质量的碳酸钠和氯化钠的饱和溶液中水的质量比较多的是NaCl |
5.下列关于溶液的说法正确的是( )
| A. | 溶液都是澄清透明无色的 | |
| B. | 碘几乎不溶于水,但可以溶解在汽油中 | |
| C. | 溶液中的溶质和溶剂都只能是一种 | |
| D. | 生理盐水中的溶质是HCl |
2.金属镍及其化合物能发生下列反应:①Ni+2HCl═NiCl2+H2↑;②NiO+2HCl═NiCl2+H2O;③NiO2+4HCl═NiCl2+Cl2↑+2H2O;分析化学方程式可知,下列说法中错误的是( )
| A. | 镍不能与硫酸铜溶液反应 | |
| B. | 反应①属于置换反应 | |
| C. | 反应③中Ni的化合价由+4价变为+2价 | |
| D. | 上述3个反应中涉及3种单质 |