题目内容
13.下列实验方法不能达到实验目的是( )| 选项 | 实验目的 | 实验操作 |
| A | 区别烧碱和食盐 | 取固体加水,并测定溶液的温度 |
| B | 检验氧气是否收集满 | 将带火星的木条放在集气瓶口,观察是否复燃 |
| C | 区别羊毛和化纤布料 | 取样品燃烧,闻气味 |
| D | 除去CO2中混有的HCl气体 | 将气体通过NaOH溶液后再通过浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据两种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们.
B、根据氧气的验满方法进行分析判断.
C、羊毛的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味,进行分析判断.
D、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、烧碱溶于水放出大量的热,食盐溶于水温度变化不大,取固体加水,并测定溶液的温度,可以鉴别,故选项实验方法能达到实验目的.
B、检验氧气是否收集满时,应将带火星的木条放在集气瓶口,观察是否复燃,故选项实验方法能达到实验目的.
C、羊毛的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味,化纤布料燃烧产生特殊的气味,可以鉴别,故选项实验方法能达到实验目的.
D、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项实验方法不能达到实验目的.
故选:D.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列化学方程式书写正确的是( )
| A. | Al+H2SO4═AlSO4+H2↑ | B. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2 | ||
| C. | 2P+5O2$\frac{\underline{\;点燃\;}}{\;}$P2O5 | D. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 |
8.过多尿素[CO(NH2)2]等进入水体会恶化水质,导致“水华”现象.尿素属于( )
| A. | 氮肥 | B. | 钾肥 | C. | 磷肥 | D. | 复合肥 |
5.婴儿“尿不湿”最关键的材料是聚丙烯酸钠,其吸水性是棉花、纸张的数十倍.它是由丙烯酸【C3H4O2】与氢氧化钠经过一系列的复杂反应而制得.下列有关丙烯酸的说法中,正确的是( )
| A. | 它是由3个碳元素,4个氢元素和2个氧元素组成 | |
| B. | 其中氧元素与氢元素的质量比为9:1 | |
| C. | 其中碳元素的质量分数为50% | |
| D. | 一个丙烯酸分子由3个碳原子、4个氢原子和1个氧分子构成 |
2. 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )
 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃时,甲乙两物质各50g分别加入100g水中充分溶解,得到的溶液质量都是140g | |
| B. | t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 | |
| C. | t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 | |
| D. | t2℃时,甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙 |
3. 按如图所示方案进行实验.下列有关说法及分析不正确的是( )
按如图所示方案进行实验.下列有关说法及分析不正确的是( )
 按如图所示方案进行实验.下列有关说法及分析不正确的是( )
按如图所示方案进行实验.下列有关说法及分析不正确的是( )| A. | 试管①中有红色固体析出 | |
| B. | 试管②中的化学方程式为2AgNO3+Fe═2Ag+Fe(NO3)2 | |
| C. | 试管①和②中的反应均属于置换反应 | |
| D. | 只要有单质生成的反应就是置换反应 |
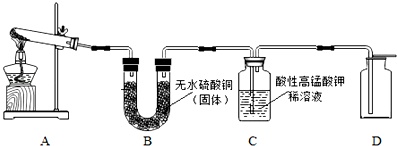
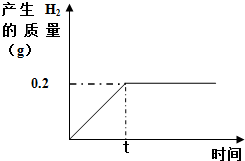 取一定质量的铁粉与100g稀硫酸反应,铁粉与稀硫酸恰好完全反应.产生的氢气随时间的变化如图所示:
取一定质量的铁粉与100g稀硫酸反应,铁粉与稀硫酸恰好完全反应.产生的氢气随时间的变化如图所示: