题目内容
14.用数轴表示某化学知识直观、简明、易记.下列用数轴表示的化学知识,错误的是( )| A. | 部分元素原子序数关系: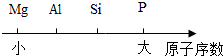 | |
| B. |  生活中常见物质的pH(常温下,中性溶液的pH为7,酸性溶液的pH<7,碱性溶液的pH>7): 生活中常见物质的pH(常温下,中性溶液的pH为7,酸性溶液的pH<7,碱性溶液的pH>7): | |
| C. | 地壳中部分元素的含量关系: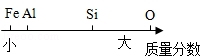 | |
| D. | 空气中部分成分的体积分数关系: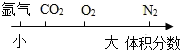 |
分析 A、根据元素原子序数分析;
B、根据常见物质pH的大小考虑;
C、根据地壳中部分元素的含量分析判断;D、根据空气中各种气体的体积分数考虑.
解答 解:A、镁、铝、硅、磷的原子序数分别为12、13、14、15,故表示正确;
B、生活中常见物质,醋酸酸性较强,pH较低,雨水一般为5.6,食盐水为中性,pH值=7,肥皂水显碱性,pH值大于7,故表示正确;
C、在地壳中元素的含量从高到低的顺序是氧硅铝铁,故表示正确;
D、空气中,氩气的体积分数大于二氧化碳的体积分数,故表示错误.
故选:D.
点评 本题考查了常见的用数轴法表示化学知识,完成此题,可以依据已有的知识进行,所以要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.

练习册系列答案
相关题目
5.下列关于溶液的说法正确的是( )
| A. | 溶液都是澄清透明无色的 | |
| B. | 碘几乎不溶于水,但可以溶解在汽油中 | |
| C. | 溶液中的溶质和溶剂都只能是一种 | |
| D. | 生理盐水中的溶质是HCl |
2.金属镍及其化合物能发生下列反应:①Ni+2HCl═NiCl2+H2↑;②NiO+2HCl═NiCl2+H2O;③NiO2+4HCl═NiCl2+Cl2↑+2H2O;分析化学方程式可知,下列说法中错误的是( )
| A. | 镍不能与硫酸铜溶液反应 | |
| B. | 反应①属于置换反应 | |
| C. | 反应③中Ni的化合价由+4价变为+2价 | |
| D. | 上述3个反应中涉及3种单质 |
9.X、Y、Z三种金属及其化合物可发生如下反应:Y+ZCl2═Z+YCl2 X+ZCl2═Z+XCl2 X+HCl不反应 Y+2HCl═YCl2+H2↑,则X、Y、Z三种金属的活动性由强到弱的顺序是( )
| A. | Z>Y>X | B. | X>Y>Z | C. | Y>X>Z | D. | Y>Z>X |
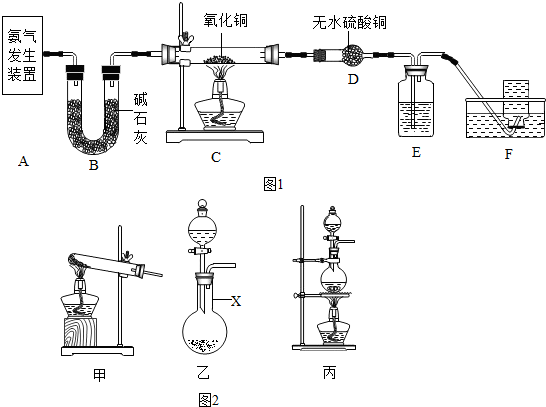
 同学们在探究物质燃烧的条件时,设计了如图所示的实验,请回答有关问题.
同学们在探究物质燃烧的条件时,设计了如图所示的实验,请回答有关问题.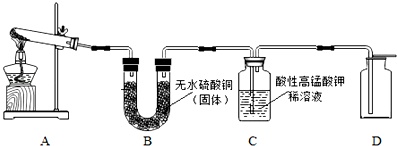
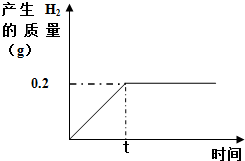 取一定质量的铁粉与100g稀硫酸反应,铁粉与稀硫酸恰好完全反应.产生的氢气随时间的变化如图所示:
取一定质量的铁粉与100g稀硫酸反应,铁粉与稀硫酸恰好完全反应.产生的氢气随时间的变化如图所示: