题目内容
13. 在实验课上,老师给同学们一包红色粉未,已知该粉末是铜粉和和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
在实验课上,老师给同学们一包红色粉未,已知该粉末是铜粉和和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.【提出问题】假设l:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;
假设3:红色粉末是铜粉和氧化铁粉的混合物.
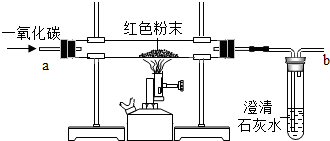
【设计方案】同学们对实验作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如图),请补全下表中空白处的现象.
| 实验中可能出现的现象 | 结论 |
| 无明显现象 | 假设1成立 |
| 红色粉末变黑色,澄清石灰水变浑浊 | 假设2成立 |
| 红色粉末部分变为黑色,石灰水变浑浊 | 假设3成立 |
【反思与评价】①实验过程中,硬质玻璃管内发生的化学反应方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②实验时通入一氧化碳片刻后再加热的原因是防止加热不纯的一氧化碳引起爆炸.
③上面的实验装置有不足之处,请你对该装置进行改进,具体措施是将尾气点燃或收集.
【拓展延伸】为了进一步探究铁和铜的金属活动性强弱,可选用下列试剂中的AB (填序号).
A.硝酸铜溶液 B.稀盐酸 C.氯化亚铁溶液.
分析 【提出问题】根据题意,对红色粉末进行猜想;
【设计实验方案】根据实验结论,分析支持结论应该出现的实验现象;
【反思与评价】对实验装置的操作进行解释及对存在问题进行改进;
【拓展】根据铁和铜的化学性质分析选择的试剂.
解答 解:【提出问题】通过分析可知,该粉末是铜粉和氧化铁粉中的一种或两种,因此红色粉末可能为两物质的混合物;
【设计实验方案】铜在高温下不与一氧化碳反应,因此粉末不变色,澄清石灰水也不会出现浑浊;氧化铁在高温下可与一氧化碳反应生成黑色铁粉和二氧化碳,充分反应后,粉末变黑色,澄清石灰水浑浊;
【反思与评价】
①一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
②一氧化碳具有可燃性,与空气混合点燃可能发生爆炸,因此应先通一氧化碳,待玻璃管内气体为纯净的一氧化碳时再进行加热,防止形成混合气体而引起爆炸;
③一氧化碳气体有毒,直接排放到空气中会造成空气污染,可把尾气进行燃烧或收集,所以可在b处用酒精灯点燃,或用塑料袋(气球)收集;
【拓展】金属铁可与硝酸铜反应,与盐酸反应生成氢气,而铜不能与硝酸铜反应,也不能与盐酸反应,所以A、B可验证铁的活动性比铜强;铁和铜都不能与氯化亚铁反应,C不能验证铁和铜的活动性.
故答案为:【提出问题】铜粉和氧化铁的混合物;
【设计方案】
| 实验中可能出现的现象 | 结论 |
| 无明显现象 | 假设1成立 |
| 红色粉末变黑色,澄清石灰水变浑浊 | 假设2成立 |
| 红色粉末部分变为黑色,澄清石灰水变浑浊 | 假设3成立 |
②防止加热不纯的一氧化碳引起爆炸;
③将尾气点燃或收集;
【拓展延伸】AB.
点评 在使用可燃性气体时,一定要注意检验气体的纯度,不纯的气体在点燃时有可能出现爆炸;可能气体主要有:氢气、一氧化碳、甲烷(天然气).

练习册系列答案
相关题目
4. 如图所示,小松同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂.为了确定盐酸与氢氧化钠是否恰好完全反应,小松同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是他得出“两种物质已恰好完全中和”的结论.
如图所示,小松同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂.为了确定盐酸与氢氧化钠是否恰好完全反应,小松同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是他得出“两种物质已恰好完全中和”的结论.
(1)中和反应的实质是氢离子和氢氧根离子结合成了水分子.中和反应在实际中具有广泛的应用,请举出一个实例用于医药,如用氢氧化铝治疗胃酸过多.
(2)对实验一反应后溶液中的溶质进行探究.
【提出猜想】猜想一:只有NaCl 猜想二:有NaCl和NaOH 猜想三:有NaCl和HCl
你认为猜想二不合理,其理由是此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】请你另设计一个实验,探究上述烧杯中的溶液是否恰好完全反应,填写下表:
 如图所示,小松同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂.为了确定盐酸与氢氧化钠是否恰好完全反应,小松同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是他得出“两种物质已恰好完全中和”的结论.
如图所示,小松同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂.为了确定盐酸与氢氧化钠是否恰好完全反应,小松同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是他得出“两种物质已恰好完全中和”的结论.(1)中和反应的实质是氢离子和氢氧根离子结合成了水分子.中和反应在实际中具有广泛的应用,请举出一个实例用于医药,如用氢氧化铝治疗胃酸过多.
(2)对实验一反应后溶液中的溶质进行探究.
【提出猜想】猜想一:只有NaCl 猜想二:有NaCl和NaOH 猜想三:有NaCl和HCl
你认为猜想二不合理,其理由是此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】请你另设计一个实验,探究上述烧杯中的溶液是否恰好完全反应,填写下表:
| 实验操作步骤 | 观察到的现象 | 结论 |
| 取少量反应后的溶液于试管中,再加入石蕊试液 | 溶液变红(或溶液不变色) | 猜想三(或一)成立 |
1.能与稀盐酸发生中和反应的是( )
| A. | 生石灰 | B. | 石灰石 | C. | KOH溶液 | D. | 锌粒 |
8.下列反应,不属于复分解反应的是( )
| A. | H2SO4+BaCl2=BaSO4↓+2HCl | B. | CaCO3+2HCl=CaCl2+CO2↑+H2O | ||
| C. | 2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O | D. | Ca(OH)2+CO2=CaCO3↓+H2O |
18.某学生用托盘天平称量固体物质时,误把固体物质放在右盘,砝码放在左盘,称得固体物质的质量为10.8g(1g以下用游码),则这位同学所称固体的实际质量是( )
| A. | 9.2g | B. | 9.8g | C. | 10.8g | D. | 10.2g |
5.小京同学今天的午餐食谱是:主食--面包;配菜和副食--炸鸡腿、炸薯片、牛排、奶酪.小京午餐缺乏的营养素是( )
| A. | 糖类 | B. | 脂肪 | C. | 蛋白质 | D. | 维生素 |
3.推理是化学学习的重要思维,下列推理符合科学事实的是( )
| A. | 氢氧化钠溶液不能敞品放置,因为氢氧化钠溶液会发生变质 | |
| B. | 置换反应会生成单质和化合物,所以生成单质和化合物的反应就是置换反应 | |
| C. | 物质能热胀冷缩,说明分子大小会随温度变化 | |
| D. | 二氧化碳通往石蕊试液中,溶液变红,说明二氧化碳是酸 |