题目内容
13.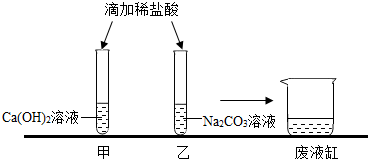 甲、乙同学在学完酸的化学性质后,做了如下实验:
甲、乙同学在学完酸的化学性质后,做了如下实验:实验结束后,甲、乙同学依次将废液缓慢倒入同一洁净的废液缸中,然后进行了讨论.
【观察与讨论1】甲同学在做实验时没有观察到明显现象,于是对氢氧化钙溶液和稀盐酸能发生反应表示怀疑.但乙同学认为,甲同学实验时向氢氧化钙溶液中应先滴几滴酚酞试液,再滴加适量的稀盐酸,当观察到(1)溶液由红色变成无色时,就可以说明两种物质能发生反应.
【观察与讨论2】当乙同学沿废液缸内壁缓慢倾倒液体时,观察到废液缸中先有气泡产生,然后又出现白色沉淀.经过讨论确定,甲、乙同学试管中废液含有的溶质分别是(2)CaCl2、HCl(写化学式),(3)NaCl、Na2CO3(写化学式),才会出现上述现象.
为了科学处理实验后产生的废液,甲、乙同学决定对废液缸中最终废液溶质的成分进行探究.
【提出问题】最终废液中含有什么溶质?
【猜想与假设】甲同学猜想:废液中含有NaCl、CaCl2两种物质;
乙同学猜想:废液中含有NaCl、Na2CO3两种两质;
【活动与探究】甲、乙同学为了验证自己的猜想分别同时进行了如下实验:
甲同学实验:取少量废液于试管中,向其中滴加碳酸钠溶液,无明显现象.
得出结论:甲猜想不成立,则乙猜想成立.
乙同学实验:取少量废液于试管中,向其中滴加氯化钙溶液,出现白色沉淀.
得出结论:乙猜想成立,则甲猜想不成立.
【表达与交流】甲、乙同学确定了最终废液中溶质的成分.你认为处理该废液的方法是(4)向废液中加入稀盐酸,直至不产生气泡为止.写出处理废液时发生的一个反应的化学方程式:(5)Na2CO3+2HCl═2NaCl+H2O+CO2↑.
分析 稀盐酸和氢氧化钙反应生成氯化钙和水,稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳;
氯化钙和碳酸钠反应生成白色沉淀碳酸钙和氯化钠;
氢氧化钙溶液显碱性,能使酚酞试液变红色,稀盐酸显酸性,不能使酚酞试液变色.
解答 解:【观察与讨论1】
氢氧化钙和稀盐酸反应时无明显现象,因此实验时向氢氧化钙溶液中应先滴几滴酚酞试液,再滴加适量的稀盐酸,当观察到溶液由红色变成无色时,就可以说明两种物质能发生反应.
故填:溶液由红色变成无色.
【观察与讨论2】
当乙同学沿废液缸内壁缓慢倾倒液体时,观察到废液缸中先有气泡产生,然后又出现白色沉淀,说明甲中稀盐酸过量,乙中碳酸钠过量,因此甲同学试管中废液含有的溶质是CaCl2、HCl,乙同学试管中废液含有的溶质是NaCl、Na2CO3.
故填:CaCl2、HCl;NaCl、Na2CO3.
【表达与交流】
最终废液中溶质的成分是NaCl、Na2CO3两种两质,处理该废液的方法是向废液中加入稀盐酸,直至不产生气泡为止,这时废液中只有一种溶质--氯化钠;
稀盐酸和碳酸钠反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故填:向废液中加入稀盐酸,直至不产生气泡为止;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
8.下列实验中无明显现象的是( )
| A. | 将浓硫酸加入蒸馏水中并不断搅拌 | B. | 向Mg(NO3)2溶液中滴加Na2SO4溶液 | ||
| C. | 向H2SO4溶液中滴加Ba(OH)2溶液 | D. | 将(NH4)2SO4和熟石灰混合研磨 |
5.某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:CuSO4溶液分别与NaOH溶液、BaCl2溶液反应.实验结束后将两实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.
(1)写出废液混合后使滤液变无色时一定发生的反应的化学方程式:CuCl2+2NaOH=Cu(OH)2↓+2 NaCl.
(2)用pH试纸测定滤液的 pH=7.
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想Ⅰ:NaCl;猜想ⅡNaCl、BaCl2;猜想ⅢNaCl、Na2SO4.
【实验探究】
【交流拓展】要使蓝色溶液变成无色,还可以用不同于上述原理的方法,即在蓝色溶液中加入足量的锌.
(1)写出废液混合后使滤液变无色时一定发生的反应的化学方程式:CuCl2+2NaOH=Cu(OH)2↓+2 NaCl.
(2)用pH试纸测定滤液的 pH=7.
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想Ⅰ:NaCl;猜想ⅡNaCl、BaCl2;猜想ⅢNaCl、Na2SO4.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 实验①:取少量滤液于试管中,加入适量的纯碱溶液,振荡. | 无明显现象 | 猜想Ⅱ不成立 |
| 实验②取少量滤液于试管中,滴加适量的BaCl2溶液(写溶质的化学式),振荡. | 产生白色沉淀 | 猜想Ⅲ成立 |
 在实验室利用如图所示装置制取气体,请回答有关问题.
在实验室利用如图所示装置制取气体,请回答有关问题.