题目内容
18.酸使石蕊变红色,是因为它的溶液中含有H+(填符号,下同);鸡蛋壳放入食醋中冒出气泡,表明鸡蛋壳中可能含有碳酸钙.分析 酸是电离时产生的阳离子全部是氢离子的化合物,酸能与活泼金属、碳酸盐等反应产生气体,据此进行分析解答即可.
解答 解:酸使石蕊变红色,是因为它的溶液中含有氢离子,其离子符号为:H+.
鸡蛋壳放入食醋中冒出气泡,食醋中含有醋酸,醋酸能与碳酸盐等反应生成气体,表明鸡蛋壳中可能含有碳酸钙.
故答案为:H+;碳酸钙.
点评 本题难度不大,掌握酸的化学性质(酸能与活泼金属、碳酸盐等反应产生气体)等是正确解答本题的关键.

练习册系列答案
相关题目
18.精美的雕花玻璃可以通过氢氟酸(HF)对玻璃的腐蚀作用制成,氢氟酸与玻璃发生反应的化学方程式为:SiO2+4HF=X↑+2H2O,则X的化学式为( )
| A. | F2 | B. | SiF4 | C. | SiH4 | D. | O2 |
6.下列图象能正确反映对应关系的是( )
| A. | 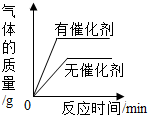 用,一定量的双氧水制取氧气 | |
| B. | 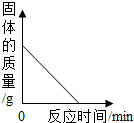 加热一定量高锰酸钾固体产生氧气 | |
| C. | 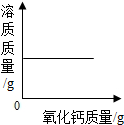 向一定量的饱和石灰水中加入氧化钙 | |
| D. |  向一定量的硝酸银溶液中插入铜丝 |
10.如图所示实验操作中正确的是( )
| A. | 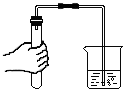 检查装置气密性 | B. | 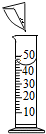 在量筒中配制溶液 | ||
| C. | 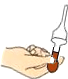 用滴管转移试剂 | D. | 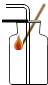 气体验满 |
7.“金银铜铁锡”俗称五金,有关五金的叙述错误的是( )
| A. | 焊锡(锡铅合金)的熔点比锡低 | |
| B. | 金属银能与硝酸铜溶液发生置换反应 | |
| C. | 金是不活泼金属,在自然界中有单质存在 | |
| D. | 钢铁应用广泛,但铁不是地壳中含量最多的金属 |
8.常温下,下列各组物质在给定条件下能大量共存的是( )
| A. | 在pH=2的溶液中:KCl、Na2SO4、HNO3 | |
| B. | 在pH=1的溶液中:NaCl、Na2CO3、Na2SO4 | |
| C. | 在pH=13的溶液中:BaCl2、Na2CO3、NaOH | |
| D. | 在pH=14的溶液中:FeCl3、Ba(NO3)2、CaCl2 |
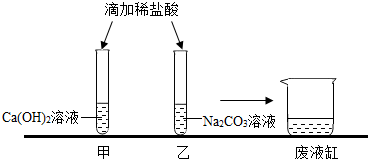 甲、乙同学在学完酸的化学性质后,做了如下实验:
甲、乙同学在学完酸的化学性质后,做了如下实验: