题目内容
10. 某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:
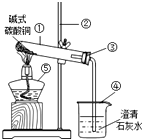
某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:实验准备:氧化铜可以利用加热碱式碳酸铜来制取
(1)试管中碱式碳酸铜加热前后的颜色变化由绿色变为黑色;
(2)烧杯中反应的文字表达式为二氧化碳+氢氧化钙→碳酸钙+水.
【实验一】
| 实验步骤 | 实验现象 | 实验结论 |
| ①在试管中加入2ml5%的过氧化氢溶液,将带火星的小木条伸入试管中 | 木条不复燃 | 在常温下,双氧水分解速率很慢 |
| ②在试管中加入2ml5%的过氧化氢溶液,加入0.1g的氧化铜,将带火星的小木条伸入试管 | 木条复燃 | 氧化铜可以加快双氧水的分解速率 |
实验目的:探究氧化铜在反应前后质量是否改变
实验步骤:在实验后,该同学将反应剩余物过滤、洗涤、干燥、称量.得到黑色固体0.1g
实验结论:氧化铜的质量在化学反应前后不变.
【实验三】
实验目的:探究氧化铜在化学反应前后化学性质是否改变
实验步骤:待步骤②试管中不再产生气泡后,继续向试管内加入2mL5%的过氧化氢溶液,伸入带火星的小木条,看到小木条复燃,说明氧化铜还能继续加快双氧水分解.
实验结论:氧化铜在反应前后化学性质不变.
分析 (1)碱式碳酸铜是一种常见绿色粉末状物质,受热可分解出氧化铜、二氧化碳和水;
(2)根据二氧化碳与氢氧化钙反应生成碳酸钙和水分析;
【实验一】根据过氧化氢的分解条件及现象分析.
【实验二】根据催化剂的探究实验分析;
【实验三】根据催化剂的特点及验证方法分析;
解答 解:(1)碱式碳酸铜是一种常见绿色粉末状物质,受热可分解出氧化铜、二氧化碳和水. 现象为绿色固体逐渐变成黑色固体,试管口产生水珠,同时生成能使澄清石灰水变浑浊的气体.
(2)烧杯中是二氧化碳与氢氧化钙的反应,二氧化碳与氢氧化钙反应生成碳酸钙和水,其文字表达式为:二氧化碳+氢氧化钙→碳酸钙+水;
【实验一】①在试管中加入2ml5%的过氧化氢溶液,将带火星的小木条伸入试管中,木条不复燃,这说明过氧化氢没分解,或生成氧气的量较少;②在试管中加入2ml5%的过氧化氢溶液,加入0.1g的氧化铜,将带火星的小木条伸入试管,木条复燃,说明氧化铜可加快过氧化氢的分解速率;
【实验二】要证明氧化铜是反应的催化剂,还要证明氧化铜的质量在反应前后是否不变,故要收集反应后的氧化铜,称量后和反应前进行比较;
【实验三】要证明氧化铜是反应的催化剂,还要证明氧化铜的化学性质在反应前后是否不变,故要重新设计实验验证反应后的氧化铜是否具有相同的性质;
故答案为:(1)绿,黑;
(2)二氧化碳+氢氧化钙→碳酸钙+水;
(3)在常温下,双氧水分解速率很慢;
氧化铜可以加快双氧水的分解速率;
(4)探究氧化铜在反应前后质量是否改变;
(5)复燃;
氧化铜在反应前后化学性质不变;
点评 了解催化剂的特点,过氧化氢的分解原理,及氧化铜可作过氧化氢反应的催化剂即可顺利解答.

练习册系列答案
相关题目
1.下列实验现象描述正确的是( )
| A. | 铜片放入硝酸银溶液中:紫红色固体表面有银白色固体析出,溶液由无色逐渐变为蓝色 | |
| B. | 打开浓盐酸试剂瓶,在瓶口有白烟产生 | |
| C. | 铁丝在空气中加热:银白色固体剧烈燃烧,火星四射,放出大量的热,生成黑色固体 | |
| D. | 铜片放入稀盐酸中:紫红色固体表面产生气泡,固体减少,溶液由无色逐渐变为蓝色,放热 |
18.下列做法中正确的是( )
| A. | 尝药品的味道 | |
| B. | 实验剩余的药品放回原试剂瓶中 | |
| C. | 加热试管里的液体时,试管口不能朝着自己或他人 | |
| D. | 用燃着的酒精灯点燃另一酒精灯 |
5.小明学习了化学知识后,感到化学很有趣,他决定制作一个“无壳鸡蛋”作为母亲生日礼物献给妈妈.他从厨房中选择鸡蛋,还应选取( )
| A. | 味精 | B. | 食盐 | C. | 白醋 | D. | 酱油 |
15. 甲、乙两种固体物质的溶解度曲线如图所示.现将两支分别装有甲、乙两种物质饱和溶液(底部均有未溶解的固体)的试管浸入盛有水的烧杯里,然后向烧杯中加入一定量的浓硫酸,则对相关变体判断正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示.现将两支分别装有甲、乙两种物质饱和溶液(底部均有未溶解的固体)的试管浸入盛有水的烧杯里,然后向烧杯中加入一定量的浓硫酸,则对相关变体判断正确的是( )
 甲、乙两种固体物质的溶解度曲线如图所示.现将两支分别装有甲、乙两种物质饱和溶液(底部均有未溶解的固体)的试管浸入盛有水的烧杯里,然后向烧杯中加入一定量的浓硫酸,则对相关变体判断正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示.现将两支分别装有甲、乙两种物质饱和溶液(底部均有未溶解的固体)的试管浸入盛有水的烧杯里,然后向烧杯中加入一定量的浓硫酸,则对相关变体判断正确的是( )| A. | 甲溶液中溶质的质量分数增大 | B. | 乙溶液中未溶解的固体质量减小 | ||
| C. | 甲、乙物质的溶解度都增大 | D. | 乙溶液中溶质的质量分数不变 |
19.下列物质属于纯净物的是( )
| A. | 生理盐水 | B. | 清洁的空气 | C. | 液态氧 | D. | 豆浆 |
20.实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出该化学反应的符号表达式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
提出猜想
除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂.
完成实验
按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
分析数据、得出结论
(1)由实验①与实验4对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是Mn02.
反思
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变;
(3)实验室也可以用分解过氧化氢溶液来制取氧气,写出该化学反应的符号表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(4)猜想:影响过氧化氢溶液分解反应的速率是催化剂的种类,试设计实验验证:催化剂种类;取浓度相同、质量相同的过氧化氢溶液分别加入不同种类的同质量的催化剂进行实验,测定收集150mL氧气所需的时间即可.
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
提出猜想
除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂.
完成实验
按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(质量比1:1) | 350 |
| ③ | KClO3、CuO(质量比1:1) | 370 |
| ④ | KClO3、Fe2O3(质量比1:1) | 390 |
(1)由实验①与实验4对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是Mn02.
反思
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变;
(3)实验室也可以用分解过氧化氢溶液来制取氧气,写出该化学反应的符号表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(4)猜想:影响过氧化氢溶液分解反应的速率是催化剂的种类,试设计实验验证:催化剂种类;取浓度相同、质量相同的过氧化氢溶液分别加入不同种类的同质量的催化剂进行实验,测定收集150mL氧气所需的时间即可.
 明朝名臣、民族英雄于谦的诗作《石灰吟》:
明朝名臣、民族英雄于谦的诗作《石灰吟》: