题目内容
18.下列做法中正确的是( )| A. | 尝药品的味道 | |
| B. | 实验剩余的药品放回原试剂瓶中 | |
| C. | 加热试管里的液体时,试管口不能朝着自己或他人 | |
| D. | 用燃着的酒精灯点燃另一酒精灯 |
分析 A、根据实验室中不能直接接触药品、不能品尝药品、不能把鼻孔直接放在试剂瓶口闻气味;
B、根据实验用剩的药品的处理原则分析;
C、根据加热试管里的液体时的注意事项进行分析;
D、根据酒精灯的点燃方法分析.
解答 解:A、有的药品有毒,不能品尝药品,故A做法不正确;
B、为防止药品污染,用剩的药品不能放回原瓶,应放入指定的回收容器中,故B做法不正确;
C、给试管里的液体加热时,防止液体飞溅伤人,试管口不能朝着有人的方向,故C做法正确;
D、点燃酒精灯要用火柴,不能用燃着的酒精灯点燃另一酒精灯,故D做法不正确.
故选C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
8.下列实验操作正确的是( )
| A. |  取用固体药品 | B. |  闻药品的气味 | ||
| C. | 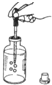 吸取液体药品 | D. |  将大理石块放入试管 |
9.从化学的角度分析,下列做法不合理的是( )
| A. | 氮气的化学性质不活泼,用于食品防腐 | |
| B. | 生活中通过煮沸可以降低水的硬度 | |
| C. | 城市道路使用的太阳能景观灯,节能又环保 | |
| D. | 采用燃烧氢气的方式生产水,补充城市饮用水资源的不足 |
6.下列有关资源或能源的叙述不正确的是( )
| A. | 地壳中含量最高的金属元素是铝,年产量最高的金属是铁 | |
| B. | 海洋中有80多种元素,是巨大的资源宝库,其中含量最多的元素是氢 | |
| C. | 回收废旧电池能节约金属资源,减少环境污染 | |
| D. | 我国是世界上已知矿物种类比较齐全的少数国家之一,钨、钛等储量居世界前列 |
10.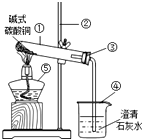 某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:
某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:
实验准备:氧化铜可以利用加热碱式碳酸铜来制取
(1)试管中碱式碳酸铜加热前后的颜色变化由绿色变为黑色;
(2)烧杯中反应的文字表达式为二氧化碳+氢氧化钙→碳酸钙+水.
【实验一】
【实验二】
实验目的:探究氧化铜在反应前后质量是否改变
实验步骤:在实验后,该同学将反应剩余物过滤、洗涤、干燥、称量.得到黑色固体0.1g
实验结论:氧化铜的质量在化学反应前后不变.
【实验三】
实验目的:探究氧化铜在化学反应前后化学性质是否改变
实验步骤:待步骤②试管中不再产生气泡后,继续向试管内加入2mL5%的过氧化氢溶液,伸入带火星的小木条,看到小木条复燃,说明氧化铜还能继续加快双氧水分解.
实验结论:氧化铜在反应前后化学性质不变.
 某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:
某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:实验准备:氧化铜可以利用加热碱式碳酸铜来制取
(1)试管中碱式碳酸铜加热前后的颜色变化由绿色变为黑色;
(2)烧杯中反应的文字表达式为二氧化碳+氢氧化钙→碳酸钙+水.
【实验一】
| 实验步骤 | 实验现象 | 实验结论 |
| ①在试管中加入2ml5%的过氧化氢溶液,将带火星的小木条伸入试管中 | 木条不复燃 | 在常温下,双氧水分解速率很慢 |
| ②在试管中加入2ml5%的过氧化氢溶液,加入0.1g的氧化铜,将带火星的小木条伸入试管 | 木条复燃 | 氧化铜可以加快双氧水的分解速率 |
实验目的:探究氧化铜在反应前后质量是否改变
实验步骤:在实验后,该同学将反应剩余物过滤、洗涤、干燥、称量.得到黑色固体0.1g
实验结论:氧化铜的质量在化学反应前后不变.
【实验三】
实验目的:探究氧化铜在化学反应前后化学性质是否改变
实验步骤:待步骤②试管中不再产生气泡后,继续向试管内加入2mL5%的过氧化氢溶液,伸入带火星的小木条,看到小木条复燃,说明氧化铜还能继续加快双氧水分解.
实验结论:氧化铜在反应前后化学性质不变.
8.相同质量的镁、铜、铁、钾中,含有原子数目最多的是( )
| A. | 镁 | B. | 铜 | C. | 铁 | D. | 钾 |
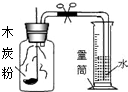 氧气是一种化学性质比较活泼的气体,它可以和许多物质发生反应例如木炭、硫粉和细铁丝都能与氧气反应.
氧气是一种化学性质比较活泼的气体,它可以和许多物质发生反应例如木炭、硫粉和细铁丝都能与氧气反应.