题目内容
19.下列物质属于纯净物的是( )| A. | 生理盐水 | B. | 清洁的空气 | C. | 液态氧 | D. | 豆浆 |
分析 纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质.据此逐项分析即可.
解答 解:A、生理盐水中含有水、氯化钠,属于混合物.故错误;
B、清洁的空气中含有氮气、氧气等多种等物质,属于混合物.故错误.
C、液态氧是由一种物质组成的,属于混合物,故正确;
D、豆浆含有水、蛋白质、油脂等多种物质,属于混合物,故错误.
故选C.
点评 解答本题要充分理解纯净物和混合物的区别,要分析物质是由几种物质组成的,如果只有一种物质组成就属于纯净物,如果有多种物质就属于混合物.

练习册系列答案
相关题目
9.从化学的角度分析,下列做法不合理的是( )
| A. | 氮气的化学性质不活泼,用于食品防腐 | |
| B. | 生活中通过煮沸可以降低水的硬度 | |
| C. | 城市道路使用的太阳能景观灯,节能又环保 | |
| D. | 采用燃烧氢气的方式生产水,补充城市饮用水资源的不足 |
10.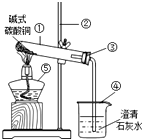 某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:
某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:
实验准备:氧化铜可以利用加热碱式碳酸铜来制取
(1)试管中碱式碳酸铜加热前后的颜色变化由绿色变为黑色;
(2)烧杯中反应的文字表达式为二氧化碳+氢氧化钙→碳酸钙+水.
【实验一】
【实验二】
实验目的:探究氧化铜在反应前后质量是否改变
实验步骤:在实验后,该同学将反应剩余物过滤、洗涤、干燥、称量.得到黑色固体0.1g
实验结论:氧化铜的质量在化学反应前后不变.
【实验三】
实验目的:探究氧化铜在化学反应前后化学性质是否改变
实验步骤:待步骤②试管中不再产生气泡后,继续向试管内加入2mL5%的过氧化氢溶液,伸入带火星的小木条,看到小木条复燃,说明氧化铜还能继续加快双氧水分解.
实验结论:氧化铜在反应前后化学性质不变.
 某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:
某化学兴趣小组为了探究氧化铜能否代替二氧化锰作为双氧水的催化剂,进行以下探究:实验准备:氧化铜可以利用加热碱式碳酸铜来制取
(1)试管中碱式碳酸铜加热前后的颜色变化由绿色变为黑色;
(2)烧杯中反应的文字表达式为二氧化碳+氢氧化钙→碳酸钙+水.
【实验一】
| 实验步骤 | 实验现象 | 实验结论 |
| ①在试管中加入2ml5%的过氧化氢溶液,将带火星的小木条伸入试管中 | 木条不复燃 | 在常温下,双氧水分解速率很慢 |
| ②在试管中加入2ml5%的过氧化氢溶液,加入0.1g的氧化铜,将带火星的小木条伸入试管 | 木条复燃 | 氧化铜可以加快双氧水的分解速率 |
实验目的:探究氧化铜在反应前后质量是否改变
实验步骤:在实验后,该同学将反应剩余物过滤、洗涤、干燥、称量.得到黑色固体0.1g
实验结论:氧化铜的质量在化学反应前后不变.
【实验三】
实验目的:探究氧化铜在化学反应前后化学性质是否改变
实验步骤:待步骤②试管中不再产生气泡后,继续向试管内加入2mL5%的过氧化氢溶液,伸入带火星的小木条,看到小木条复燃,说明氧化铜还能继续加快双氧水分解.
实验结论:氧化铜在反应前后化学性质不变.
14.下列有关实验的描述正确的是( )
| A. | 人体呼出气体的主要成分是二氧化碳和水蒸气 | |
| B. | 燃烧的木条可以用于检验二氧化碳和氮气 | |
| C. | 氢气验纯时,发出尖锐爆鸣声说明不纯 | |
| D. | 蜡烛在空气中燃烧产生大量白烟 |
4.小明利用红磷测定空气中氧气的体积分数,实验后发现测得氧气的体积分数低于$\frac{1}{5}$,针对这一现象,你认为下列做法或想法不可取的是( )
| A. | 查看实验装置是否漏气 | |
| B. | 可能是红磷的量不足,没有将瓶内氧气消耗尽 | |
| C. | 实验中可能未冷却至室温就打开止水夹,使进入瓶内水的体积减少 | |
| D. | 实验结果相差不多无需再重做实验 |
11.下列物质按混合物 纯净物 单质 氧化物顺序排列的是( )
| A. | 空气 冰水 金刚石 氯酸钾 | |
| B. | 洁净的空气 氯化钠 液氧 蒸馏水 | |
| C. | 稀有气体 海水 铁 氧化铝 | |
| D. | 澄清石灰水 水银 氦气 二氧化碳 |
8.相同质量的镁、铜、铁、钾中,含有原子数目最多的是( )
| A. | 镁 | B. | 铜 | C. | 铁 | D. | 钾 |