题目内容
15.某小组同学利用如图所示装置探究铁生锈的条件(铁锈可视为Fe2O3•nH2O),其中C、D的分液漏斗中为足量且浓度和体积均相同的稀盐酸.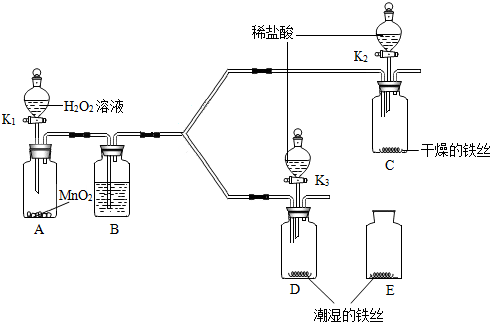
(1)步骤一:关闭K2和K3,打开K1,A中反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,B中所盛放的试剂是浓硫酸.对比铁丝表面的变化,能够说明铁生锈与水有关的是装置CD(填C、D或E,下同),能够说明铁生锈的快慢与氧气浓度有关的是装置DE.
(2)步骤二:关闭K1,打开K2和K3,将装置C、D中分液漏斗内的稀盐酸同时全部注入广口瓶中,C中发生的化学反应方程式为Fe+2HCl=FeCl2+H2↑,充分反应后D的溶液中一定含有FeCl3(填化学式).
分析 根据探究铁生锈的条件结合化学方程式的书写分析;根据题中提供的信息分析研究铁生锈的条件;
钢铁生锈的条件是钢铁与氧气和水同时接触.根据反应物和生成物及其质量守恒定律可以书写化学方程式
解答 解:(1)可以用过氧化氢和二氧化锰混合制取氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
因为收集氧气时,可以用浓硫酸干燥.对比铁丝表面的变化,能够说明铁生锈与水可以用干燥和潮湿两种铁丝;铁生锈的快慢与氧气浓度有关的是纯净氧气和空气中的氧气;
(2)铁单独与氧气接触或与水接触时不容易生锈,与水和氧气同时接触时容易生锈.故C中铁不生锈,其化学方程式是Fe+2HCl=FeCl2+H2↑;D中铁生锈,生成氧化铁,与盐酸反应生成氯化铁;
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. 浓硫;C D; D E;
(2)Fe+2HCl=FeCl2+H2↑;FeCl3
点评 解答本题要掌握化学方程式的书写方法、氧气的制取及其铁生锈的条件等方面的知识,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.化学用语书写正确的是( )
| A. | 硝酸镁-MgNO3 | B. | 1个二氧化硫分子-SO2 | ||
| C. | 3个氧原子-O3 | D. | 铵根-NH3 |
3.下列物质由分子构成的是( )
| A. | 铜 | B. | 氯化钠晶体 | C. | 硅 | D. | 干冰 |
10.下列实验所对应的方案正确的是( )
| 选项 | 目的 | 方案 |
| A | 除去木炭粉中的氧化铜 | 在空气中充分燃烧 |
| B | 分离NaCl和CaCO3的混合物 | 加足量稀盐酸,蒸发 |
| C | 区分稀盐酸和稀氢氧化钠溶液 | 分别测溶液的pH |
| D | 鉴别化肥NH4Cl和NH4NO3 | 取样,加熟石灰研磨 |
| A. | A | B. | B | C. | C | D. | D |
7.只用一种试剂来鉴别氯化钠、氯化钡、稀盐酸三种溶液,这种试剂是( )
| A. | 碳酸钠溶液 | B. | 稀硫酸 | C. | 无色酚酞溶液 | D. | 紫色石蕊溶液 |

 当今,染发已经成为一种时尚,年轻人可以随自己的心情和喜好改变头发的颜色,给人眼前一亮的感觉.但是它在给予我们美丽的同时,会对我们的健康造成伤害,染发剂中的染料具有一定的毒性、刺激性和过敏性.例如,染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用.因此,科学界告诫我们:慎用染发剂,少染发为好.
当今,染发已经成为一种时尚,年轻人可以随自己的心情和喜好改变头发的颜色,给人眼前一亮的感觉.但是它在给予我们美丽的同时,会对我们的健康造成伤害,染发剂中的染料具有一定的毒性、刺激性和过敏性.例如,染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用.因此,科学界告诫我们:慎用染发剂,少染发为好.